Перейти к:
Сохранение и укрепление репродуктивного здоровья работающих граждан. Методические рекомендации
https://doi.org/10.15829/3034-4123-2024-8
EDN: HTUNFA
Аннотация
Методические рекомендации разработаны с целью упорядочения, систематизации и определения ключевых направлений для реализации на уровне работодателей отдельных мероприятий или комплексной корпоративной программы сохранения и укрепления репродуктивного здоровья работающих граждан, в том числе с учетом международного опыта.
Методические рекомендации содержат описание семи ключевых подпрограмм, направленных на раннюю диагностику и своевременное лечение заболеваний мочевыделительной системы, оценку репродуктивного здоровья для создания семьи, повышение грамотности в вопросах полового воспитания и поведения, снижение негативного воздействия факторов производственной и внешней среды на репродуктивное здоровье, повышение приверженности мерам борьбы с факторами риска развития хронических неинфекционных заболеваний, поддержку в периоды наступления менопаузы у женщин и андропаузы у мужчин, а также создание условий на рабочем месте, благоприятствующих сохранению крепкой семьи. Методические рекомендации предназначены для специалистов в области организации здравоохранения и общественного здоровья, руководителей органов государственной власти субъектов Российской Федерации в сфере охраны здоровья, специалистов региональных центров общественного здоровья и медицинской профилактики, а также для руководителей организаций различных отраслей экономической деятельности, в том числе при взаимодействии с ними в рамках реализации положений о проведении работникам профилактических медицинских осмотров, диспансеризация и диспансерного наблюдения по месту осуществления гражданами служебной деятельности. Материалы, представленные в методических рекомендациях, также могут быть использованы медицинскими работниками различных специальностей (фельдшерами фельдшерскоакушерских пунктов и здравпунктов, врачами-терапевтами участковыми, врачами общей практики (семейными врачами), врачами-акушерами-гинекологами, врачами-дерматовенерологами, врачами по медицинской профилактике, врачами-профпатологами и врачами-урологами).
Ключевые слова
Для цитирования:
Драпкина ОМ, Орлов СА, Шепель РН, Концевая АВ, Аполихин ОИ, Красняк СС, Долгушина НВ, Залата ИВ, Лебедева НА, Победенная ГП, Шарапова ЮА. Сохранение и укрепление репродуктивного здоровья работающих граждан. Методические рекомендации. Первичная медико-санитарная помощь. 2024;1(1):81-133. https://doi.org/10.15829/3034-4123-2024-8. EDN: HTUNFA
For citation:
Drapkina OM, Orlov SA, Shepel RN, Kontsevaya AV, Apolikhin OI, Krasnyak SS, Dolgushina NV, Zalata IV, Lebedeva NA, Pobedennaya GP, Sharapova YA. Reproductive health promotion in working individuals. Guidelines. Primary Health Care (Russian Federation). 2024;1(1):81-133. (In Russ.) https://doi.org/10.15829/3034-4123-2024-8. EDN: HTUNFA
Введение
В рамках реализации Концепции демографической политики Российской Федерации на период до 2025 г., утвержденной Указом Президента Российской Федерации от 9 октября 2007 г. № 1351 (далее — Концепция), а также плана мероприятий по ее реализации в 2021-2025 гг., утвержденного распоряжением Правительства Российской Федерации от 16 сентября 2021 г. № 2580-р (далее — План мероприятий), реализуются программы, направленные на:
— укрепление репродуктивного здоровья населения;
— обеспечение доступности и повышение качества медицинской помощи по восстановлению репродуктивного здоровья, в том числе с использованием вспомогательных репродуктивных технологий;
— поэтапное сокращение рабочих мест с тяжелыми, вредными и опасными для репродуктивного здоровья населения условиями труда и проведение мероприятий по профилактике и своевременному выявлению профессиональных заболеваний.
В настоящее время в Российской Федерации:
— активно внедряются современные методы диагностики, направленные на увеличение охвата женщин, которым проводится оценка антенатального развития плода на сроке беременности 11-14 нед.;
— увеличивается раннее выявление заболеваний у детей, включая скрининговые программы, в том числе до рождения ребенка, расширяются программы неонатального и пренатального скринингов на наследственные и врожденные заболевания;
— увеличивается охват подростков в возрасте 15-17 лет профилактическими медицинскими осмотрами с целью сохранения их репродуктивного здоровья;
— растет доля женщин, прошедших доабортное консультирование с целью сохранения беременности, а также женщин, которым оказана социальная, юридическая и психологическая помощь в ходе доабортного консультирования, позволяющая им сохранить беременность;
— повышается доступность медицинской помощи пациентам, страдающим бесплодием, путем применения вспомогательных репродуктивных технологий;
— растет раннее выявление в ходе диспансеризации и профилактических осмотров у молодых женщин хронических заболеваний, которые могут приводить к бесплодию, и обеспечивается своевременное оказание медицинской помощи.
Кроме того, с 2022 г. работодателями ведется разработка и внедрение программ профилактики заболеваний на рабочих местах, формирования здоровой среды на производствах, направленных преимущественно на профилактику развития хронических неинфекционных заболеваний (ХНИЗ).
Вместе с тем в контексте указанных Концепции и Плана мероприятий, Указа Президента Российской Федерации от 22.11.2023 № 875 "О проведении в Российской Федерации Года семьи", а также положений Указа Президента Российской Федерации от 7 мая 2024 г. № 309 "О национальных целях развития Российской Федерации на период до 2030 года и на перспективу до 2036 года", положений Плана основных мероприятий по проведению в Российской Федерации Года семьи от 26 декабря 2023 г. № 21515-П45-ТГ, разрабатываемых и планируемых к реализации с 2025 г. национальных проектов "Семья" и "Продолжительная и активная жизнь" особый акцент должен быть сделан на создании условий по сохранению и укреплению репродуктивного здоровья не только на уровне государственных программ, но и найти отражение в отдельных мероприятиях или корпоративных программах укрепления здоровья работающих граждан на уровне каждой организации (предприятия), в том числе с учетом ее отраслевой специфики и особенностей производственных процессов.
Целью настоящих методических рекомендаций является упорядочение, систематизация и определение ключевых направлений для реализации на уровне работодателей отдельных мероприятий или комплексной корпоративной программы сохранения и укрепления репродуктивного здоровья работающих граждан, в том числе с учетом международного опыта.
Среди основных направлений (подпрограмм), которые рекомендуется учитывать работодателям при подготовке комплексной корпоративной программы или при реализации отдельных мероприятий, обеспечивающих сохранение и укрепление репродуктивного здоровья работающих граждан, могут быть выделены следующие:
— обеспечение возможности для работников по ранней диагностике и своевременному лечению заболеваний мочевыделительной системы;
— обеспечение возможности для работников по проведению оценки репродуктивного здоровья для создания семьи;
— проведение мероприятий по повышению грамотности в вопросах полового воспитания и поведения;
— создание условий для минимизации воздействия факторов производственной и внешней среды, оказывающих влияние на репродуктивное здоровье;
— реализация мер, направленных на борьбу с факторами риска развития ХНИЗ, оказывающих влияние на репродуктивное здоровье;
— оказание комплексной поддержки в периоды наступления менопаузы у женщин и андропаузы у мужчин;
— создание условий на рабочем месте по обеспечению родителям психологического, социального и финансового стимулирования за рождение детей и реинтеграции матерей в рабочую среду.
1.1. ПОДПРОГРАММА "РАННЯЯ ДИАГНОСТИКА И СВОЕВРЕМЕННОЕ ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ МОЧЕВЫДЕЛИТЕЛЬНОЙ СИСТЕМЫ"
АКТУАЛЬНОСТЬ
Среди наиболее часто встречающихся причин, прямо или косвенно оказывающих влияние на репродуктивное здоровье населения, выделяются заболевания мочеполовой системы инфекционной и неинфекционной этиологии. Прежде всего необходимо выделить инфекции нижних мочевыводящих путей, вызывающие такое заболевание, как цистит. Существуют различные формы цистита:
Интерстициальный цистит (синдром боли в мочевом пузыре) представляет собой изнурительное заболевание, характеризующееся частыми тазовыми болями и сопровождающееся сексуальной дисфункцией (диспареуния, изменение полового влечения и частоты оргазмов, недостаточное выделение смазки) [1]. Интерстициальный цистит чаще поражает женщин, при этом, несмотря на сложность в оценке распространенности данного заболевания, эксперты предполагают, что на каждые 100 тыс. женщин может быть выявлено от 10 до 500 случаев [2]. По некоторым оценкам, распространенность данного заболевания в настоящее время достигает 25% у женщин и более 8% у мужчин [3].
Посткоитальный цистит — воспалительное заболевание мочевого пузыря, развивающееся после полового акта. На фоне циститов после полового акта с постоянными обострениями пациентки нередко отказываются от половой жизни, наступает выраженная сексуальная дисфункция [4].
Еще одной серьезной и распространенной медико-социальной проблемой у женщин репродуктивного возраста является недержание мочи, которое, по данным эпидемиологических исследований, составляет от 10 до более 40% [5]. Около 350 млн человек во всем мире страдают недержанием мочи [6], что отрицательно влияет на общее качество жизни женщин, но также было показано отрицательное влияние на женскую сексуальную функцию (около 26% женщин со стрессовой и примерно 43% со смешанной формой недержания мочи отмечает, что данное состояние негативно влияет на их сексуальные отношения). Женщины со стрессовым недержанием мочи значительно чаще испытывают снижение либидо (отношение шансов (OR)=1,96), сухость влагалища (OR=2,11) и диспареунию (OR=2,04) независимо от возраста [7].
Бессимптомная бактериурия также встречается очень часто. Среди здоровых молодых женщин, ведущих активную половую жизнь, распространенность бессимптомной бактериурии составляет около 1,5% возрасте 20 лет, увеличиваясь до 3-5% к 50 годам [8] и до 10-20% у женщин к 80 годам, при этом редко встречаясь у мужчин в возрасте после 50 лет. Женщины с бессимптомной бактериурией, выявленной на ранних сроках беременности и не получающие лечения, имеют риск развития пиелонефрита на более поздних сроках беременности от 20 до 30% [8].
Пиелонефрит — наиболее распространенная тяжелая бактериальная инфекция, осложняющая беременность. Пиелонефрит поражает 1-2% беременных и связан со значительной заболеваемостью матери и плода. Антенатальный пиелонефрит сопряжен с преждевременным излитием околоплодных вод, преждевременными родами, низкой массой тела при рождении и недоношенностью [9]. Примерно у 20% женщин с тяжелым пиелонефритом развиваются осложнения, включающие синдром септического шока или его предполагаемые варианты (дисфункция почек, гемолиз и тромбоцитопения, а также повреждение легочных капилляров) [10].
Хроническая болезнь почек (ХБП) часто сопровождается проблемами репродуктивного здоровья как у женщин, так и у мужчин. Прогрессирование ХБП связано с нарастающим нарушением гипоталамо-гипофизарно-гонадной оси, что способствует развитию дисфункции яичников, яичек и сексуальной функции. К частым клиническим осложнениям репродуктивного здоровья при ХБП относятся нарушения менструального цикла, нарушения сексуального здоровья и снижение фертильности [11]. Женщины с ХБП сталкиваются со сложными решениями и серьезными проблемами в репродуктивном возрасте. Среди женщин с ХБП риски беременности значительны: риск преэклампсии в 10 раз выше, а риск преждевременных родов — в 6 раз [12].
ЦЕЛЬ ПОДПРОГРАММЫ
Обеспечить в организации проведение информационной кампании по вопросам профилактики, диагностики и лечения заболеваний мочеполовой системы и дать возможность работникам пройти необходимое обследование у профильных врачей-специалистов в медицинской организации при наличии соответствующих симптомов или имеющихся заболеваний.
ОПИСАНИЕ
При реализации подпрограммы в организации рекомендуется:
1) издать распорядительный документ о проведении информационной кампании и обязать всех сотрудников организации принять участие в данном мероприятии;
2) проинформировать региональный центр общественного здоровья и медицинской профилактики о готовности к проведению на территории организации информационной кампании в формате лекции совместно с соответствующими врачами-специалистами (врач-уролог, врач-нефролог, врач-акушер-гинеколог);
3) разработать совместно с региональным центром общественного здоровья и медицинской профилактики форму обратной связи от сотрудников организации об эффективности формата информационной кампании и доступности полученных знаний;
4) обеспечить возможность работникам организации пройти необходимое медицинское обследование в медицинской организации, оказывающей первичную медико-санитарную помощь (ПМСП), для диагностики и лечения (при необходимости) выявленного заболевания мочеполовой системы.
Реализация подпрограммы не требует дополнительного финансирования. Мероприятия информационной кампании выполняются за счет средств, предусмотренных в рамках финансового обеспечения деятельности региональных центров общественного здоровья и медицинской профилактики, а медицинское обследование в целях выявления заболеваний мочеполовой системы — за счет средств обязательного медицинского страхования (ОМС) в рамках реализации территориальной программы государственных гарантий бесплатного оказания гражданам медицинской помощи.
Для реализации подпрограммы необходимо:
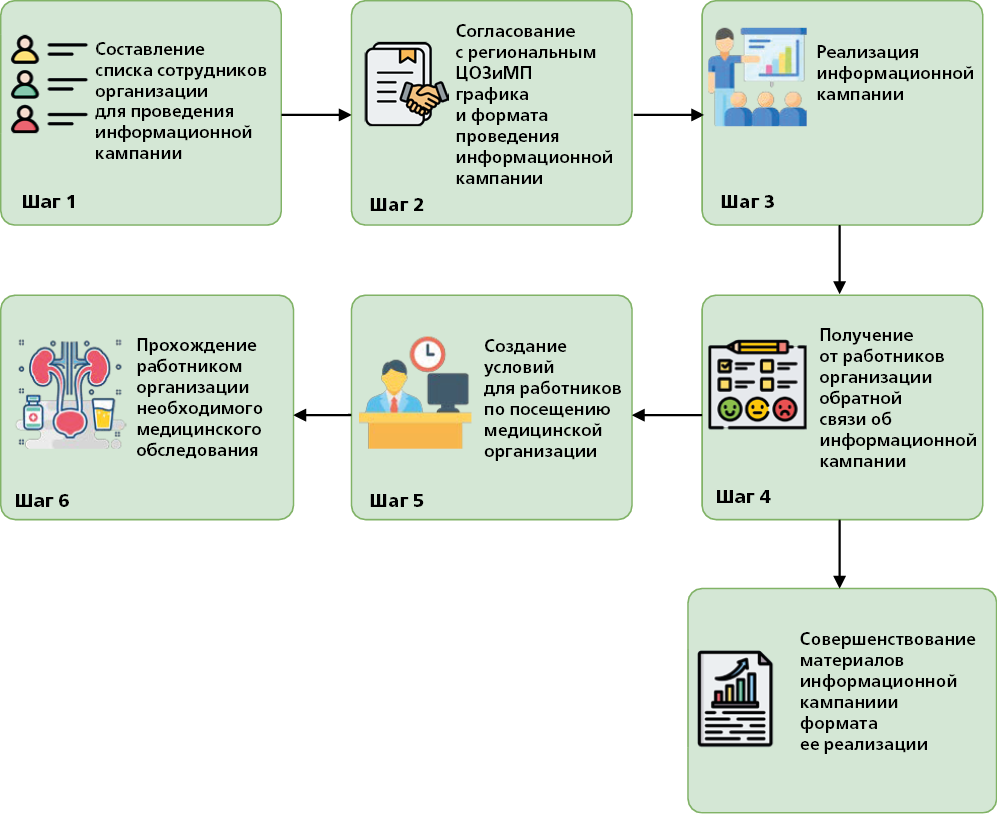
ОТВЕТСТВЕННЫЕ
— руководитель кадровой службы организации (менеджер по персоналу);
— руководитель регионального Центра общественного здоровья и медицинской профилактики;
— руководитель медицинской организации, оказывающей ПМСП, в которой проводится диагностика и лечение (при необходимости) заболеваний мочеполовой системы.
СРОКИ РЕАЛИЗАЦИИ
Проведение информационной кампании — регулярно, не реже 1 раза в календарном году.
Ссылка на материалы — после реализации информационной кампании с регулярным обновлением по мере совершенствования образовательного контента.
ИНДИКАТОРЫ РЕЗУЛЬТАТА
Для работодателя и организации:
- Доля работников организации, принявших участие в информационной кампании от всех работников организации. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, удовлетворенных качеством и доступностью материалов, представленных в рамках информационной кампании, от всех работников организации. Рекомендуется, чтобы данный показатель составлял не менее 85%.
Для системы здравоохранения:
- Доля работников организации, посетивших медицинскую организацию, оказывающую ПМСП, в целях диагностики заболеваний мочевыделительной системы от числа работников, проявивших настороженность в отношении наличия у них заболеваний мочевыделительной системы. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, приверженных лечению заболеваний мочевыделительной системы, от числа работников, которым данные заболевания диагностированы. Рекомендуется, чтобы данный показатель составлял не менее 85%.
1.2. ПОДПРОГРАММА "ОЦЕНКА РЕПРОДУКТИВНОГО ЗДОРОВЬЯ ДЛЯ СОЗДАНИЯ СЕМЬИ"
АКТУАЛЬНОСТЬ
Распространенность бесплодия у женщин репродуктивного возраста составляет одну из каждых семи пар в западном мире и одну из каждых четырех пар в развивающихся странах. Бесплодием страдают от 8 до 12% пар репродуктивного возраста во всем мире [13], при этом на долю мужчин в целом приходится 50% случаев [14]. По данным федеральной статистической отчетности, в Российской Федерации в настоящее время зарегистрировано около 300 тыс. человек, страдающих бесплодием.
Около 7% мужчин во всем мире имеют диагноз мужского бесплодия, которое может быть результатом низкой выработки спермы, нарушения функции спермы или барьеров, препятствующих попаданию спермы в матку. Болезни, травмы, долгосрочные проблемы со здоровьем, выбор образа жизни и другие факторы могут привести к мужскому бесплодию. Согласно последним исследованиям, в мужской популяции наблюдается глобальное снижение количества сперматозоидов, что усиливает дискуссию о мужской фертильности. За последние 50 лет количество сперматозоидов у мужчин сократилось во всем мире более чем на 50% [13][14], при этом негативная тенденция продолжается — количество сперматозоидов у мужчин во всем мире снижается ускоренными темпами — на 2,64% в год [15]. При сохранении текущего сценария количество сперматозоидов значительно снизится к 2045 г.
Бесплодные мужчины имеют более высокий риск рака (например, яичка, простаты, лимфомы, молочной железы) и других неблагоприятных последствий для здоровья, таких как болезни системы кровообращения, сахарный диабет и аутоиммунные заболевания (псориаз, системная красная волчанка, болезнь Грейвса, тиреоидит, рассеянный склероз), чем фертильные мужчины [16]. Среди ведущих заболеваний, ассоциированных с мужским бесплодием, выделяются простатит и варикоцеле.
Простатит считается наиболее распространенной урологической проблемой у мужчин моложе 50 лет и третьим по распространенности урологическим диагнозом у мужчин старше 50 лет. Общая распространенность простатита в течение жизни составляет около 14% [17]. На фоне простатита развивается сексуальная дисфункция (эякуляторная и эректильная), приводящая к мужскому бесплодию.
Варикоцеле у детей обычно диагностируется случайно, в то время как у большинства взрослых оно диагностируется во время обследования на предмет мужского фактора бесплодия. Несмотря на то, что только 20% пациентов с варикоцеле страдают проблемами фертильности, варикоцеле обнаруживается примерно у 40% пациентов с первичным бесплодием и у 80% — со вторичным бесплодием [18][19]. Варикоцеле может приводить к субфертильности по причине развития у пациента тестикулярной гипоксии, апоптоза зародышевых клеток, окислительного стресса, рефлюкса токсических метаболитов почек/надпочечников, гипертонии в семенных венах и повышения температуры яичек [20].
В настоящее время в мире насчитывается от 72,4 до 120,6 млн женщин в возрасте 20-44 лет, живущих в браке или в отношениях по обоюдному согласию, у которых бесплодие определяется как задержка зачатия на более чем 12 мес. без использования противозачаточных средств при регулярной половой жизни [21].
Наметившаяся общемировая тенденция к позднему деторождению также является причиной сокращения репродуктивного потенциала. В большинстве европейских стран средний возраст матери при рождении первого ребенка приближается к 30 годам, и многие женщины рожают первого ребенка в возрасте 35 лет и старше [22]. Существует довольно универсальная закономерность возрастного снижения рождаемости: потеря фертильности у женщин медленно увеличивается с 4,5% в возрасте 25 лет, 7% — в возрасте 30 лет, 12% — в возрасте 35 лет и 20% — в возрасте 38 лет. После этого он быстро возрастает примерно до 50% в возрасте 41 года, почти 90% в возрасте 45 лет и приближается к 100% в возрасте 50 лет [14].
На женскую фертильность также оказывает влияние наличие таких заболеваний или состояний, как:
— преждевременная недостаточность яичников (встречается примерно у 1% женщин и характеризуется прекращением менструального цикла в возрасте до 40 лет при наличии повышенного уровня фолликулостимулирующего гормона (ФСГ) в сыворотке);
— синдром поликистозных яичников (гетерогенное состояние, являющееся наиболее распространенным эндокринным заболеванием у женщин, им страдают 5-10% женского населения);
— эндометриоз (патологический воспалительный процесс органов малого таза, общая распространенность которого варьируется от 0,8 до 6%; однако у женщин с бесплодием распространенность значительно выше и колеблется от 20 до 50% со значительными вариациями в зависимости от периода времени и возраста пациенток);
— миома матки и полипы эндометрия;
— олигоменорея или аменорея, ановуляция, плохое качество гамет, дисфункция гипоталамуса.
ЦЕЛЬ ПОДПРОГРАММЫ
Обеспечить информирование работодателей и работников организаций репродуктивного возраста о возможности прохождения диспансеризации с целью оценки репродуктивного здоровья (далее — репродуктивная диспансеризация), а также обеспечить условия для ее выполнения прежде всего на рабочем месте.
ОПИСАНИЕ
При реализации подпрограммы в организации рекомендуется:
1) подготовить список работников (женщины и мужчины в возрасте 18-49 лет) для проведения репродуктивной диспансеризации;
2) обеспечить взаимодействие с региональным центром общественного здоровья и медицинской профилактики и медицинской организацией, оказывающей первичную медико-санитарную помощь, с целью планирования проведения репродуктивной диспансеризации;
3) выделить необходимое помещение для размещения медицинских работников и необходимого медицинского оборудования или обеспечить возможность размещения на территории мобильного медицинского комплекса для проведения диспансеризации с целью оценки репродуктивного здоровья;
4) организовать непрерывный поток работников организации для прохождения репродуктивной диспансеризации.
При невозможности проведения репродуктивной диспансеризации на рабочем месте работодателю рекомендуется согласовать сроки ее проведения в условиях медицинской организации, оказывающей ПМСП, спланировав поток работников таким образом, чтобы их ежедневное количество не превышало 40-50 человек (суммарно мужчин и женщин).
Реализация подпрограммы не требует дополнительного финансирования. Мероприятия репродуктивной диспансеризации выполняются согласно требованиям методических рекомендаций Минздрава России по диспансеризации мужчин и женщин репродуктивного возраста с целью оценки репродуктивного здоровья за счет средств ОМС в рамках реализации территориальной программы государственных гарантий бесплатного оказания гражданам медицинской помощи.
Для реализации подпрограммы необходимо:
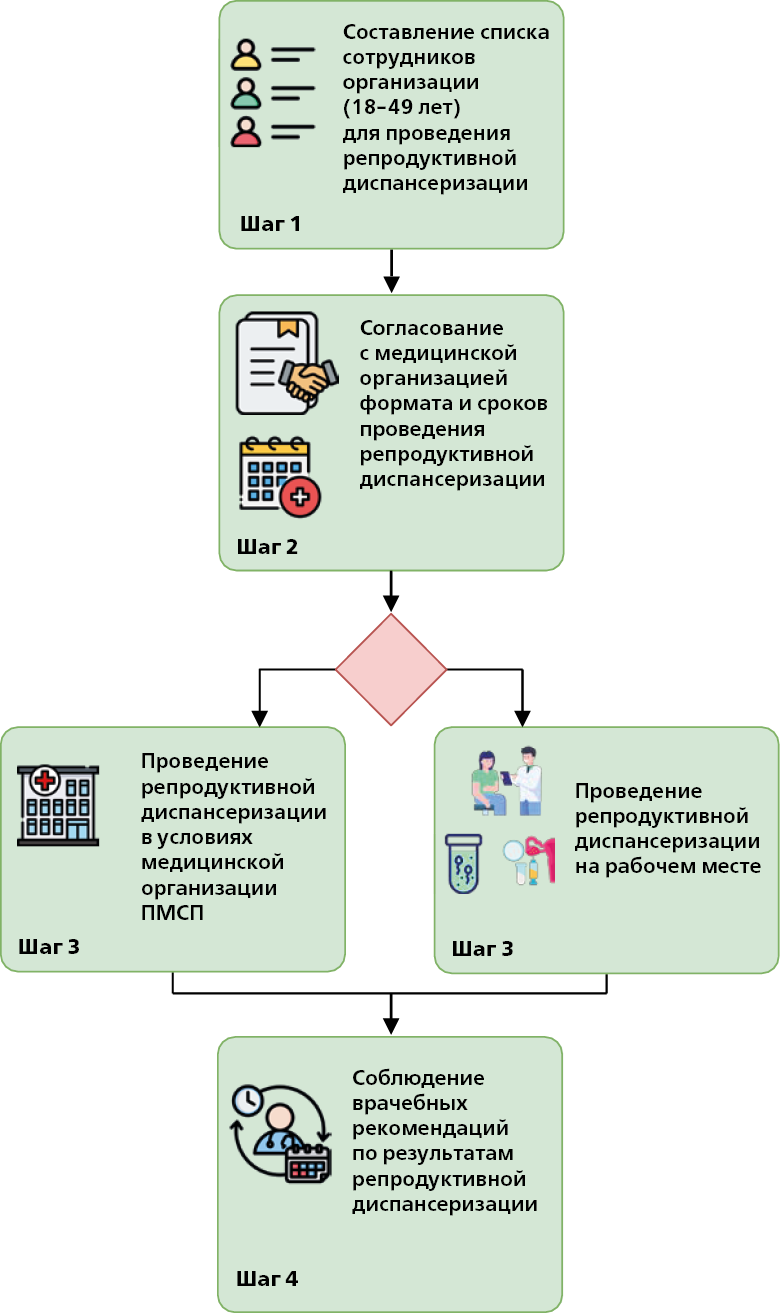
ОТВЕТСТВЕННЫЕ
— руководитель кадровой службы организации (менеджер по персоналу);
— руководитель регионального Центра общественного здоровья и медицинской профилактики;
— руководитель медицинской организации, оказывающей ПМСП, в которой проводится репродуктивная диспансеризация.
СРОКИ РЕАЛИЗАЦИИ
Ежегодно, 1 раз в год для каждого работника организации в возрасте 18-49 лет.
ИНДИКАТОРЫ РЕЗУЛЬТАТА
Для работодателя и организации:
- Доля работников организации в возрасте 18-49 лет, направленных на прохождение репродуктивной диспансеризации, от общей численности работников организации данной возрастной группы. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, пришедших в медицинскую организацию, оказывающую ПМСП (пришедших к месту проведения на работе), для прохождения репродуктивной диспансеризации, от направленных для ее прохождения. Рекомендуется, чтобы данный показатель составлял не менее 85%.
Для системы здравоохранения:
- Доля работников организации, завершивших первый этап репродуктивной диспансеризации, которым установлена соответствующая группа репродуктивного здоровья.
- Доля женщин, прошедших II этап репродуктивной диспансеризации, от числа женщин, направленных на него по результатам I этапа репродуктивной диспансеризации.
- Доля женщин, отнесенных ко II группе репродуктивного здоровья, проходящих соответствующее лечение у профильного врача-специалиста.
- Доля женщин, отнесенных к III группе репродуктивного здоровья, состоящих на диспансерном наблюдении у врача-акушера-гинеколога и которым составлена индивидуальная программа лечения.
- Доля мужчин, отнесенных ко II группе репродуктивного здоровья, посетивших в течение 6 месяцев врача-уролога для диагностики и лечения, а также обратившихся в Центр здоровья для углубленного профилактического консультирования.
- Доля мужчин, отнесенных к III группе репродуктивного здоровья, посетивших врача-уролога, имеющего дополнительное образование (имеющего практический опыт) в области андрологии/диагностики и лечения заболеваний мужской репродуктивной системы, и получивших соответствующее лечение по профилю заболевания согласно клиническим рекомендациям.
1.3. ПОДПРОГРАММА "ПОВЫШЕНИЕ ГРАМОТНОСТИ В ВОПРОСАХ ПОЛОВОГО ВОСПИТАНИЯ И ПОВЕДЕНИЯ"
АКТУАЛЬНОСТЬ
Высокая частота встречаемости заболеваний репродуктивной сферы обусловлена их ассоциацией с инфекциями, передаваемыми половым путем (ИППП) [23]. К группе данных заболеваний относятся: вирус папилломы человека (ВПЧ), вирусные гепатиты B и C, вирус иммунодефицита человека (ВИЧ), генитальный герпес, сифилис, бактериальные уретриты и цервициты (вызванные Neisseria gonorrhoeae, Chlamydia trachomatis, Mycoplasma genitalium, Trichomonas vaginalis), вагиниты, бактериальный вагиноз, трихомониаз и кандидоз.
Ежегодно во всем мире регистрируется 357 млн новых случаев четырех излечимых ИППП, среди людей в возрасте 15-49 лет. Данный показатель имеет тенденцию к росту по оценкам Всемирной организации здравоохранения в 2019 г. произошло 376 млн новых случаев заражения хламидиозом, гонореей, сифилисом и трихомониазом [24]. Данные возбудители обуславливают развитие острых воспалительных заболеваний органов малого таза (ОВЗМТ). Примерно у 15% женщин с ОВЗМТ развивается трубное бесплодие, а количество эпизодов ОВЗМТ прямо пропорционально риску бесплодия [25]. Трубное бесплодие входит в число наиболее распространенных причин бесплодия, на его долю приходится 30% проблем с фертильностью у женщин [26].
Уретрит у мужчин, вызванный такими микроорганизмами, как Chlamydia trachomatis, Neisseria gonorrhoeae, Mycoplasma genitalium, Mycoplasma hominis, при отсутствии своевременного лечения может стать причиной развития осложнений, включая острый эпидидимита, орхит и простатит, являясь одной из основных проблем здоровья, связанных с репродуктивной и половой функцией, а также ведущей причиной мужского бесплодия [27][28].
Вирус папилломы человека является одним из наиболее важных вирусов, передающихся половым путем, вызывая рак шейки матки [29]. Рак шейки матки является вторым по распространенности раком у женщин в группе злокачественных новообразований репродуктивной системы и молочной железы, более 290 млн женщин во всем мире инфицированы ВПЧ, что соответствует 570 тыс. случаев рака шейки матки и 311 тыс. связанных с ним смертей во всем мире [30][31].
Уровень распространенности ВПЧ среди мужчин составляет по различным оценкам и на основании данных, полученных в ходе научных исследований от 3,5 до 45% [32]. Исследования показали значительную корреляцию между инфекцией ВПЧ и снижением фертильности. По последним данным, ВПЧ-инфекция может быть обнаружена в сперме и связана с 10,2% случаев мужского бесплодия [33].
Во всем мире получают распространение программы скрининга с использованием чувствительных и специфичных методов диагностики, в том числе тесты амплификации нуклеиновых кислот, а также экспресс-тесты, которые могут быть использованы в корпоративной программе как элемент ранней диагностики и своевременного выявления ИППП.
ЦЕЛЬ ПОДПРОГРАММЫ
Повысить уровень информированности и грамотности работников организации в вопросах полового воспитания и поведения, применения методов барьерной контрацепции и необходимости регулярного обследования на ИППП.
ОПИСАНИЕ
При реализации подпрограммы в организации рекомендуется:
1) издать распорядительный документ о проведении информационной кампании и обязать всех сотрудников организации принять участие в данном мероприятии;
2) проинформировать региональный центр общественного здоровья и медицинской профилактики о готовности к проведению на территории организации информационной кампании в формате лекции совместно с соответствующими врачами-специалистами (врач-дерматовенеролог, врач-уролог, врач-акушер-гинеколог);
3) разработать совместно с региональным центром общественного здоровья и медицинской профилактики форму обратной связи от сотрудников организации об эффективности формата информационной кампании и доступности полученных знаний;
4) обеспечить работников организации тест-системами для экспресс-анализа на ИППП, а также медицинскими изделиями для самостоятельного сбора образцов биологического материала;
5) регулярно информировать работников организации о необходимости использования средств барьерной контрацепции (презервативов) в целях профилактики передачи ИППП;
6) обеспечить:
— в рамках проведения репродуктивной диспансеризации определение в биологическом материале микроорганизмов, вызывающих заболевания, передающиеся половым путем (ЗППП) (приоритетно);
— за счет работодателя возможность работникам организации пройти необходимые дополнительные лабораторные и инструментальные исследования в медицинской организации, оказывающей ПМСП, в том числе на анонимной основе, в целях диагностики и лечения (при необходимости) выявленного ЗППП (при наличии возможности у работодателя).
Реализация подпрограммы может потребовать дополнительного финансирования со стороны работодателя, связанного с необходимостью обеспечения работников организации соответствующими тест-системами и медицинскими изделиями, а также оплаты услуг медицинской организации по проведению дополнительных лабораторных и инструментальных исследований для диагностики ЗППП.
Для реализации подпрограммы необходимо:
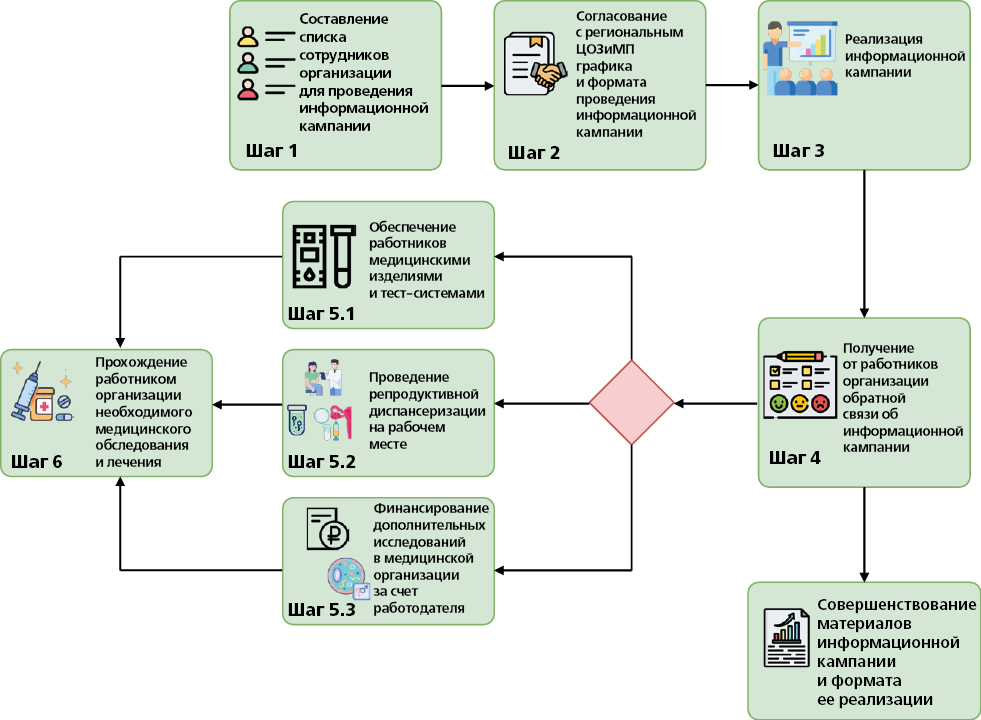
ОТВЕТСТВЕННЫЕ
— руководитель кадровой службы организации (менеджер по персоналу);
— руководитель регионального Центра общественного здоровья и медицинской профилактики;
— руководитель медицинской организации, оказывающей ПМСП, в которой проводятся лабораторные и инструментальные исследования, в том числе на анонимной основе, в целях диагностики и лечения (при необходимости) выявленного ЗППП.
СРОКИ РЕАЛИЗАЦИИ
Проведение информационной кампании — регулярно, не реже 1 раза в календарном году.
Ссылка на материалы — после реализации информационной кампании с регулярным обновлением по мере совершенствования образовательного контента.
ИНДИКАТОРЫ РЕЗУЛЬТАТА
Для работодателя и организации:
- Доля работников организации, принявших участие в информационной кампании от всех работников организации. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, удовлетворенных качеством и доступностью материалов, представленных в рамках информационной кампании, от всех работников организации. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, проявивших настороженность в отношении наличия у них ЗППП, от всех работников организации.
- Уровень обеспеченности работников организации тест-системами для экспресс-анализа на ЗППП, а также медицинскими изделиями для самостоятельного сбора образцов биологического материала. Рекомендуется, чтобы данный показатель составлял не менее 50%.
- Уровень финансового обеспечения для проведения лабораторных и инструментальных исследований ЗППП за счет средств работодателя. Рекомендуется, чтобы в организации были предусмотрены средства для оплаты не менее 50% случаев.
Для системы здравоохранения:
- Доля работников организации, посетивших медицинскую организацию, оказывающую ПМСП, в целях диагностики ЗППП из числа работников, проявивших настороженность в отношении наличия у них данных заболеваний и (или) выявивших их при помощи тест-систем для экспресс-анализа. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, приверженных лечению ЗППП, от числа работников, которым данные заболевания диагностированы. Рекомендуется, чтобы данный показатель составлял не менее 85%.
1.4. ПОДПРОГРАММА "ПРОИЗВОДСТВЕННАЯ И ВНЕШНЯЯ СРЕДА ДЛЯ РЕПРОДУКТИВНОГО ЗДОРОВЬЯ"
АКТУАЛЬНОСТЬ
К настоящему времени проведено большое количество исследований в отношении оценки влияния химических [34-36] и физических факторов на репродуктивное здоровье. Доказано негативное влияние на здоровье работников и на плод беременной женщины, в том числе тератогенного характера, следующих химических веществ [37]:
Свинец. Воздействие свинца на женскую репродуктивную функцию проявляется главным образом нарушением менструального цикла, снижением потенциала фертильности, задержкой времени зачатия и изменения выработки и циркуляции половых гормонов, оказывая влияние на беременность и ее исход [38]. Сообщаемые эффекты от воздействия свинца также включали нарушение менструального цикла, развитие бесплодия, самопроизвольных абортов и угроз выкидыша, ранний разрыв плодных оболочек, преэклампсию, гипертонию беременных и преждевременные роды [38]. Воздействие свинца связано с гормональным дисбалансом, вызывающим репродуктивные нарушения, а накопление свинца влияет на многие эндокринные железы [39]. Он влияет на гипоталамо-гипофизарную ось, вызывая притупление реакций тиреотропного гормона, гормона роста и ФСГ, лютеинизирующего гормона (ЛГ) на стимуляцию тиреотропин-рилизинг-гормона, гормона роста-рилизинг-гормона и гонадотропин-рилизинг-гормона.
Свинец снижает мужскую фертильность через снижение либидо, сперматогенеза, качества спермы, а также выработки и регуляции гормонов. Генерация избыточного количества активных форм кислорода из-за воздействия свинца потенциально влияет на жизнеспособность, подвижность сперматозоидов, фрагментацию дезоксирибонуклеиновой кислоты (ДНК) и хемотаксис для слияния сперматозоидов с ооцитами, и все это может способствовать сдерживанию оплодотворения [40]. В целом был сделан вывод, что воздействие низких и умеренных уровней свинца в окружающей среде влияет на определенные репродуктивные параметры [41]. Уровни свинца в крови >40 мкг/дл связаны с нарушением мужской репродуктивной функции, возможно за счет уменьшения количества, объема и плотности сперматозоидов или за счет изменения подвижности и морфологии сперматозоидов. Общее количество сперматозоидов снижается по мере увеличения содержания свинца в крови, а концентрации свинца в сперме демонстрируют обратную связь с общим количеством сперматозоидов, объемом эякулята и уровнем тестостерона в сыворотке [42].
Ртуть. У женщин ртуть может накапливаться в яичниках и вызывать изменения репродуктивного поведения, бесплодие и недостаточность яичников [43][44]. Повышенные дозы ртути увеличивают потенциальное количество репродуктивных нарушений (бесплодия, мертворождения, врожденных пороков развития и самопроизвольных абортов) [45]. Повышенный уровень ртути связан с бесплодием или недостаточностью фертильности. Воздействие ртути связано с увеличением частоты менструальных и гормональных нарушений, а также увеличением частоты неблагоприятных репродуктивных исходов [46]. Доказано, что у женщин ртуть оказывает ингибирующее действие на высвобождение ЛГ и ФСГ передней долей гипофиза [47][48]. Это может изменить уровень эстрогена и прогестерона, вызывая болезненные или нерегулярные менструации, перекос матки, преждевременную менопаузу и часто различные дисфункции яичников. Воздействие ртути связано с множественными нарушениями менструального цикла, такими как сокращение или удлинение менструальных циклов, аномальное кровотечение или боль [48].
Более высокие концентрации ртути в крови и волосах были связаны с мужским бесплодием [49]. Имеются доказательства того, что все параметры качества спермы были ниже у субъектов с высоким уровнем ртути и что бесплодные мужчины с аномальными параметрами спермы имели значительно более высокие концентрации ртути в крови, чем фертильные мужчины [50]. Также доказано, что концентрации ртути в семенной жидкости положительно коррелируют с аномальной морфологией сперматозоидов, а также отрицательно коррелируют с нормальной подвижностью сперматозоидов [51]. Имеются также научные исследования, демонстрирующие, что воздействие ртути из окружающей среды может привести к увеличению повреждения ДНК сперматозоидов [52].
Кадмий. Экспериментальные данные показали, что воздействие кадмия влияет на женскую фертильность, изменяя овуляцию, стероидогенез, функцию гипофиза и оплодотворение [53]. Кадмий уменьшает количество растущих фолликулов, вызывает их атрезию, изменяет структуру фолликулярных клеток, снижает овариальный резерв, уровни ФСГ и ЛГ, увеличивает продолжительность овариального цикла [54]. Кроме того, было обнаружено, что кадмий влияет на созревание фолликулов, вызывает лютеолиз [42] и утолщает эндометрий [42][55].
Кадмий у мужчин вызывает изменения семенных канальцев, клеток Сертоли, гемато-тестикулярного барьера и потерю сперматозоидов, изменяет развитие и функцию клеток Лейдига и индуцирует развитие опухоли из данных клеток. Кроме того, кадмий нарушает сосудистую систему яичка. Будучи индуктором активных форм кислорода, кадмий также вызывает повреждение ДНК и впоследствии приводит к мужской субфертильности или бесплодию [56].
Медь. Исследования показали, что медь обладает эстрогеноподобной активностью и является металлоэстрогеном. У женщин с болезнью Вильсона (высоким содержанием меди в организме) часто возникает аменорея или олигоменорея, что может быть частично связано с изменениями активности гормонов, индуцированных ионами меди [57].
Медь является медиатором окислительного стресса и играет важную роль в сперматогенезе и мужском бесплодии. Высокое воздействие ионов меди приводит к уменьшению количества сперматозоидов, подвижности сперматозоидов и количества сперматозоидов нормальной формы [58, 59]. Воздействие избыточного количества соединений меди также вызывает тератозооспермию, астенозооспермию и ухудшение качества спермы [60].
Мышьяк. Оказывает влияние на репродуктивные гормоны, воздействуя на половые железы и снижая качество спермы [61]. Репродуктивная токсичность мышьяка связана с нарушением сперматогенеза и обусловлена воздействием на ЛГ, регулирующий созревание сперматозоидов, а также на ФСГ, тестостерон и его концентрацию в яичках [62]. Мужчины, подвергшиеся воздействию неорганического мышьяка, имели плохое качество спермы (объем спермы, концентрация и подвижность сперматозоидов, целостность акросом, жизнеспособность сперматозоидов и т.д.) и эректильную дисфункцию [63-66]. Было также обнаружено, что мужчины, живущие в районах с высокой концентрацией мышьяка, являются олигозооспермическими или азооспермическими [67].
Воздействие мышьяка изменяет баланс высвобождения нейромедиаторов и гормонов, связанный с развитием и функционированием женской репродуктивной системы. Мышьяк подавляет стероидогенез яичников, удлиняет диэстральную фазу эстрального цикла, дегенерирует клетки, связанные с фолликулом яичника (фолликулярная атрезия), усиливает хромосомные аберрации в ооцитах, уменьшает дробление и предимплантационный рост, изменяет секрецию гонадотропных гормонов, которые играют важную роль в делении, дифференцировке и созревании фолликулов яичников, овуляции фолликулов яичников, формировании желтого тела, поддержании желтого тела и сохранении беременности [57].
Никель. Вызывает образование активных форм кислорода, приводя к окислительному стрессу, оказывая негативное влияние на белки и ДНК и вызывая репродуктивную токсичность. Никель отрицательно влияет на репродуктивное здоровье людей и животных [68-70]. Доказано, что наночастицы никеля влияют на уровень гормонов ФСГ и ЛГ у женщин и тестостерона у мужчин, повреждает ткани яичников и яичек [68]. Известно, что никель оказывает влияние на эндокринную систему и репродуктивные способности человека, воздействуя на гонады [71]. Существует множество информации об ассоциации воздействия никеля и развитием мужского [72] и женского бесплодия [73].
Марганец. Обладает способностью воздействовать на гены, регулирующие гипоталамический гонадотропин-рилизинг гормон, что может стимулировать его препубертатное высвобождение из гипоталамуса, ускоряя половое созревание. Высокие уровни марганца в сыворотке крови связаны с повышенным риском плохого качества спермы [74]. Подтверждено, что высокие уровни марганца связаны с повышенным риском низкой подвижности и низкой концентрации сперматозоидов [75]. У мужчин, профессионально подвергавшихся воздействию марганца, возрастает уровень ЛГ и снижается уровень тестостерона [76].
Кроме перечисленных тяжелых металлов существует множество иных химических веществ и соединений, оказывающих негативное влияние как на репродуктивное здоровье мужчин и женщин, так и на здоровье плода. Так, репродуктивная токсичность полихлорированных дифенилов (ПХД) для женщин проявляется изменением функции яичников и изменением уровня половых гормонов, ранним наступлением менопаузы, изменением менструальной функции, увеличением риска выкидыша и увеличением времени, необходимого для наступления беременности [77-80]. Воздействие ПХД на мужчин связано со снижением уровня циркулирующих репродуктивных гормонов, качества спермы (концентрация, количество, подвижность и морфология сперматозоидов, целостность их ДНК) [81-85]. Накопление ПХБ также связано с развитием рака яичек [86]. ПХД могут передаваться от матери к плоду через плаценту [87], что приводит к трансгенерационным эффектам [88][89], таким как наследственные эпимутации в сперме и мозге [90]. Пренатальное воздействие ПХД влияет на продолжительность беременности и массу тела при рождении [91, 92], а также вызывает снижение коэффициента интеллекта и плодовитости потомства [93-95].
Еще одной группой химических веществ, оказывающих токсическое действие на репродуктивное здоровье, являются органические растворители. Многие органические растворители являются известными тератогенами и эмбриотоксинами, работы с которыми во время беременности повышают риск развития серьезных аномалий у плода [96]. Обзоры литературы указывают на связь между высоким воздействием некоторых органических растворителей и риском потери плода [97]. Исследования, проведенные в отношении таких растворителей как бензол, толуол, ксилолом показали ассоциацию с возникновением скелетных пороков развития [ATSDR, editor. Toxicological profiles. Atlanta, GA: U. S. Department of Health and Human Services, Public Health Service; 2011. Toxicological Profiles (of acetone, benzene, Stoddart solvent, toluene and xylene), 98]. Воздействие толуола в 8 раз увеличивает общий риск для потомства женщин, прежде всего в части развития желудочно-кишечных и почечно-мочевых дефектов [99]. Воздействие толуола также было предложено как объяснение более высокой вероятности возникновения расщелины рта у новорожденных женщин, работающих в кожевенной и обувной промышленности [100][101]. Повышенный риск возникновения расщелин ротовой полости также связан с использованием нескольких различных классов органических растворителей [102, 103]. Воздействие органических растворителей на женщин повышает риск самопроизвольных абортов [104], приводит к развитию у плода пороков аортального и митрального клапанов сердца [105, 106], а на мужчин — к развитию у плода дефектов нервной трубки [107].
Существует также большое количество химических веществ, влияющих на работу эндокринной системы и репродуктивную функцию:
Бисфенол А (BPA) — химическое вещество, широко используемое в производстве прозрачной жесткой пластмассы, которая называется поликарбонат, для изготовления различных товаров, например бутылочек для детей или многоразовых бутылок для воды. Эпидемиологические данные свидетельствуют о том, что BPA действует на человека также, как агонист эстрогена [108], вызывая в том числе развитие ожирения [109]. BPA может мешать нормальному развитию нервной системы плода [110]. У мужчин, подвергшихся профессиональному воздействию BPA, наблюдалось снижение частоты половых актов, усиление эякуляторной дисфункции, снижение удовлетворенности своей сексуальной жизнью, снижение полового влечения и снижение способности к эрекции [108].
Фталаты — используются во многих потребительских целях, включая продукты личной гигиены, такие как лосьоны или шампуни, часто в качестве "ароматизаторов", а также в качестве пластификаторов для изменения физических характеристик базовых пластмасс, включая продукты, изготовленные из поливинилхлорида, такие как напольные покрытия, занавески для душа, упаковка и некоторое медицинское оборудование. Исследования продемонстрировали возможное неблагоприятное воздействие фталатов на репродуктивную функцию, включая связь с плохим качеством спермы и выкидышами [111][112]. Пренатальное воздействие фталатов, измеряемое по уровням их метаболитов в материнской моче, было связано с аномальным развитием мужских половых органов у плода [113][114].
Антипирены — еще один класс химикатов, предположительно токсичных для репродуктивной системы. Полибромдифениловые эфиры широко используются в пенопластах и пластмассах, а их пренатальное воздействие связано с неблагоприятными последствиями для развития нервной системы у потомства [115].
Перфторированные соединения, используемые для гидроизоляции, защиты от пятен и смазки, а также содержащиеся в упаковке пищевых продуктов и посуде с антипригарным покрытием, также снижают фертильность и вызывают бесплодие [116], вступая во взаимодействие с рецепторами эстрогена и андрогена, гормонами щитовидной железы и нейротрансмиттерами.
Пестициды (инсектициды, фунгициды и гербициды) действуют как эндокринные разрушители, нарушая секрецию и функцию репродуктивных гормонов, таких как тестостерон и ЛГ, и, как следствие, влияя на сперматогенез [117]. Среди женщин, проживающих в районах, загрязненных пестицидами, отмечается более высокий уровень неблагоприятных исходов беременности, таких как самопроизвольные аборты и преждевременные роды [118]. Доказана также взаимосвязь между снижением коэффициента плодовитости и воздействием пестицидов. Занятость родителей в сельском хозяйстве и их регулярный контакт с пестицидами может повысить риск врожденных пороков развития, таких как родимые пятна в виде гемангиомы, орофациальные расщелины, нарушения нервной системы и дефекты опорно-двигательного аппарата [119].
Помимо химических веществ существенное влияние на репродуктивное здоровье оказывают физические факторы: высокие температуры, вибрация, ионизирующее и неионизирующее излучение.
Влияние высоких температур окружающей среды отрицательно влияет на качество спермы, включая уменьшение объема спермы, количества и концентрации сперматозоидов [120]. Каждое повышение температуры яичек на 1°C приводит к снижению сперматогенеза на 14% [121]. Высокая температура окружающей среды резко снижает подвижность сперматозоидов за счет снижения активности митохондрий, синтеза аденозинтрифосфата [122] и повреждения ДНК [123], что приводит к развитию мужского бесплодия [124]. Имеется большое количество доказательств, связывающих воздействие тепла на беременных женщин с повышенным риском мертворождения, преждевременных родов, низкого веса при рождении и развитием врожденных дефектов [125][126]. Воздействие высоких температур может снижать женскую фертильность за счет ускорения старения яичников [127].
Негативное влияние на репродуктивную функцию также оказывает вибрация. Вибрация считается стрессором окружающей среды, который может повлиять на репродуктивную систему мужчин [128]. Это связано с высокой распространенностью зарегистрированных случаев ухудшения качества спермы (снижение количества морфологически нормальных сперматозоидов) среди водителей, занятых на промышленных и сельскохозяйственных работах, а также среди водителей такси [129]. Потенциальный механизм воздействия вибрации на репродуктивную систему заключается в нарушении кровообращения в тканях яичек, атрофии и изменениях температуры [123].
Ионизирующее излучение может оказывать неблагоприятное воздействие на репродуктивную функцию человека, которое зависит от дозы, продолжительности, интенсивности и частоты [130][131]. Облучение яичников дозой 4 Гр может вызвать 30% бесплодия у молодых женщин и 100% бесплодие у женщин старше 40 лет. При облучении органов малого таза также возникает сильное воздействие на матку, вызывающее задержку роста у девочек препубертатного возраста и нарушение расширения матки во время беременности с последующими выкидышами и преждевременными родами. Облучение центральной нервной системы может повлиять на сроки наступления полового созревания, привести к гиперпролактинемии или вызвать дефицит гонадотропинов, если в поле радиации вовлекается гипоталамо-гипофизарная ось [132]. Прямое облучение яичка в более низких дозах влияет на зародышевый эпителий: дозы облучения более 0,35 Гр вызывают аспермию, которая может быть обратимой. Время, необходимое для восстановления, увеличивается с увеличением дозы; однако при дозах, превышающих 2 Гр, аспермия может стать постоянной. При более высоких дозах облучения (>15 Гр) также будет нарушена функция клеток Лейдига [133][134].
Воздействие неионизирующего излучения оказывает вредное воздействие на ооциты, фолликулы яичников, ткань эндометрия, эстральный цикл, репродуктивные эндокринные гормоны, развивающийся эмбрион и развитие плода [135]. Неионизирующее излучение также увеличивает нагрузку свободных радикалов в матке и яичниках, что приводит к торможению роста клеток и нарушениям ДНК, что может привести к бесплодию [135]. Исследования показывают корреляцию между воздействием электромагнитного излучения и параметрами спермы, демонстрируя, что роль отрицательного влияния на потенциал фертильности [136][137]. Наиболее распространенными источниками неионизирующего излучения являются сотовые телефоны, ноутбуки, Wi-Fi и микроволновые печи, которые могут способствовать мужскому бесплодию. Излучение мобильного телефона вредит мужской фертильности, влияя на различные параметры, такие как подвижность сперматозоидов, количество сперматозоидов, морфология сперматозоидов, концентрация спермы, морфометрические отклонения, повышенный окислительный стресс, а также вызывает некоторые гормональные изменения [138].
ЦЕЛЬ
Обеспечить соответствие рабочих мест государственным нормативным требованиям по охране труда, минимизировать риск воздействия производственных факторов на репродуктивное здоровье работников организаций, расширить участие врачей-специалистов и перечень необходимых исследований, не выполняемых в рамках периодических медицинских осмотров, за счет реализации подпрограммы по репродуктивной диспансеризации.
ОПИСАНИЕ
При реализации подпрограммы в организации рекомендуется:
1) обеспечить аттестацию рабочих мест с комплексной оценкой условий труда (оценить соответствие гигиеническим нормативам, обеспеченность работников средствами индивидуальной защиты).
2) издать распорядительный документ о проведении информационной кампании и обязать всех сотрудников организации принять участие в данном мероприятии;
3) проинформировать региональный центр общественного здоровья и медицинской профилактики о готовности к проведению на территории организации информационной кампании в формате лекции совместно с соответствующими врачами-специалистами (врач-акушер-гинеколог, врач-профпатолог, врач-уролог);
4) провести информационную кампанию среди работников организаций, осуществляющих работы с вредными и (или) опасными производственными факторами о необходимости прохождения репродуктивной диспансеризации в дополнение к периодическим медицинским осмотрам 1;
5) разработать совместно с региональным центром общественного здоровья и медицинской профилактики форму обратной связи от сотрудников организации об эффективности формата информационной кампании и доступности полученных знаний.
Реализация подпрограммы не требует дополнительного финансирования.
Для реализации подпрограммы необходимо:
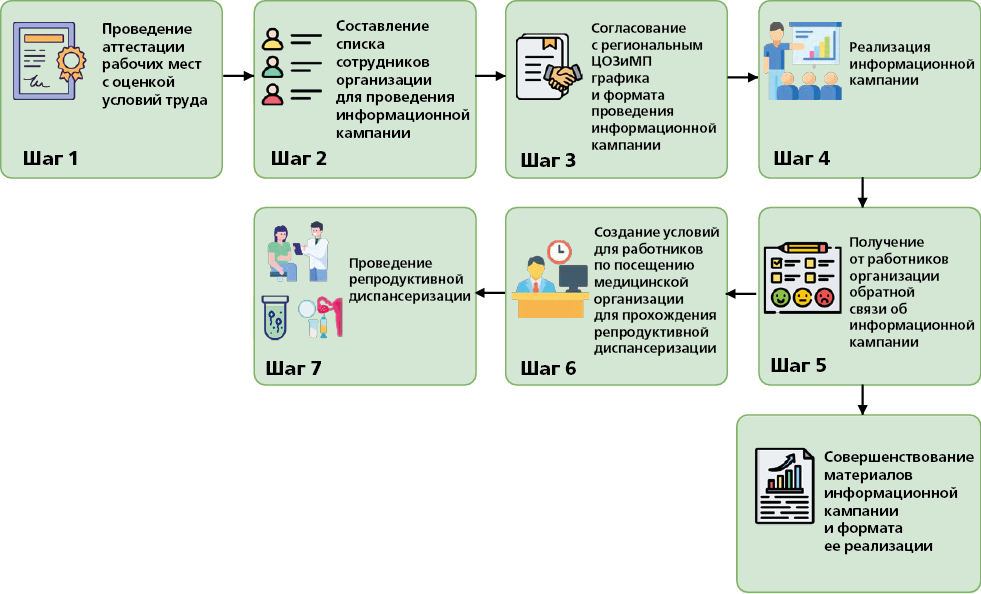
ОТВЕТСТВЕННЫЕ
— руководитель кадровой службы организации (менеджер по персоналу);
— руководитель регионального Центра общественного здоровья и медицинской профилактики;
— руководитель медицинской организации, выполняющей периодический медицинский осмотр и (или) репродуктивную диспансеризацию.
СРОКИ РЕАЛИЗАЦИИ
Согласно периодичности осмотров, установленной Приказом 2.
ИНДИКАТОРЫ РЕЗУЛЬТАТА
Для работодателя и организации:
- Доля работников организации, принявших участие в информационной кампании от всех работников организации. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, удовлетворенных качеством и доступностью материалов, представленных в рамках информационной кампании, от всех работников организации. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, осуществляющих работы с вредными и (или) опасными производственными факторами, пришедшие в медицинскую организацию, оказывающую ПМСП, для прохождения репродуктивной диспансеризации, от всех работников организации. Рекомендуется, чтобы данный показатель составлял не менее 70%.
Для системы здравоохранения:
- Доля работников организации, осуществляющих работы с вредными и (или) опасными производственными факторами, приверженных лечению заболеваний репродуктивной сферы, от числа работников, которым данные заболевания диагностированы. Рекомендуется, чтобы данный показатель составлял не менее 85%.
1.5. ПОДПРОГРАММА "РЕПРОДУКТИВНОЕ ЗДОРОВЬЕ БЕЗ ФАКТОРОВ РИСКА ХРОНИЧЕСКИХ НЕИФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ"
АКТУАЛЬНОСТЬ
Среди факторов риска развития ХНИЗ, которые также оказывают значительное влияние на репродуктивное здоровье населения, выделяются курение, употребление алкоголя, нерациональное питание, избыточная масса тела или ожирение, низкая физическая активность (малоподвижный образ жизни) и психоэмоциональный стресс.
Курение влияет на несколько аспектов женской репродуктивной функции и, следовательно, на естественную женскую фертильность, оказывая множественное дифференциальное воздействие на несколько органов-мишеней: яичник, маточные трубы и матку [139-141]. Сигаретный дым содержит около 4 000 веществ, принадлежащих к различным химическим классам, в том числе полициклические ароматические углеводороды, тяжелые металлы и алкалоиды — соединения, обладающие репродуктивной токсичностью. Большинство исследований демонстрируют данные о повышении распространенности бесплодия или недостаточности фертильности у курящих женщин, риск бесплодия у которых на 60% выше, чем у некурящих [142]. Курение во время беременности также влияет на фертильность потомства женского пола [143]. В большинстве исследований у курящих женщин, воспользовавшихся вспомогательными репродуктивными технологиями, были обнаружены значительно более низкие шансы клинической беременности и более высокие шансы внематочной беременности [144-146], а также отмечено, что пассивное курение столь же вредно, как и активное курение, в отношении имплантации и частоты наступления беременности [147]. Курение является наиболее постоянным и установленным независимым фактором риска для наступления естественной менопаузы в более молодом возрасте [148][149] с предполагаемым воздействием примерно на один год [149], что обусловлено его ингибирующим влиянием на рост фолликулов. У курящих женщин отмечаются более низкие уровни эстрогенов и прогестерона [150][151] и более высокие уровни андрогенов [152-154] в циркулирующей крови, а также более низкие уровни эстрогенов и повышенное соотношение андрогенов/эстрогенов в фолликулярной жидкости [155]. Механизмы, связанные с курением, также ставят под угрозу эффективность заместительной терапии эстрогенами [156]. У заядлых курильщиц повышен риск олигоменореи, причем риск выше у женщин, приближающихся к менопаузе, чем у более молодых женщин [157]. Интенсивное курение связано с повышенным риском укорочения менструальных циклов (менее 25 дней) [158]. Курение связано с повышенной вероятностью более продолжительной сильной боли в течение менструального цикла [159][160] и умеренно повышенным риском развития хронической дисменореи [161]. Как активное, так и пассивное курение связано со значительно более высокими рисками внематочной беременности [162-165], при этом значительно увеличивается вероятность одной или нескольких внематочных беременностей у активных курильщиц в репродуктивном возрасте, а также у некурящих женщин, подверженных высокому уровню пассивного воздействия табачного дыма в течение жизни по сравнению с некурящими без пассивного воздействия табачного дыма. Кроме того, курение влияет как на рецептивность эндометрия, так и на пролиферацию, миграцию и инвазию цитотрофобластов, тем самым определяя задержку имплантации эмбриона в матку [165-168].
У мужчин-курильщиков наблюдаются изменения морфологии и снижение концентрации, подвижности и жизнеспособности сперматозоидов [169][170]. Механизмы, приводящие к нарушению параметров спермы, связаны с возникновением ультраструктурных аномалий сперматозоидов, которые наблюдаются у заядлых курильщиков [171][172]; аналогичным образом, курение ухудшает акросомную реакцию [173] и капацитацию [174] — два процесса, которые необходимы для оплодотворения. Повышенный окислительный стресс, а также гипоксия, возникающая в результате курения сигарет, также могут быть причиной нарушения сперматогенеза [175][176]. Еще в 2012 г. Американское общество репродуктивной медицины отмечало, что "параметры спермы и результаты функциональных тестов сперматозоидов у курильщиков на 22% хуже, чем у некурящих, и зависят от количества выкуриваемых сигарет" [177]. Данные 2016 г. [178] подтвердили результаты ранее проведенных исследований, показав, что у умеренных и заядлых курильщиков с большей вероятностью снижается количество и подвижность сперматозоидов.
Алкоголь оказывает хорошо известное пагубное воздействие на женщин во время беременности, провоцируя выкидыши, мертворождение или расстройства алкогольного спектра плода [179]. Исследования, проведенные в отношении исследования влияния алкоголя на женскую фертильность, показали, что у женщин с высоким (более 7 порций алкоголя в неделю) употреблением алкоголя увеличивается время наступления беременности [180], а при употреблении алкоголя от 1 до 90 г. в неделю отмечается снижение частоты зачатий более чем на 50% в менструальном цикле [181]. Как умеренное (0-1 порция в день), так и высокое (более 1 порции в день) потребление алкоголя значительно увеличивает риск овуляторного бесплодия [182]. Потребление любого количества алкоголя (0-7+ порций в неделю) является значимым предиктором бесплодия среди женщин старше 30 лет [183]. Даже умеренное употребление алкоголя влияет на эндокринный профиль у женщин репродуктивного возраста путем повышения уровня эстрогенов и подавления уровня прогестерона [184]. Употребление алкоголя может влиять на половое созревание, вызывать нарушение регулярности менструального цикла и ановуляцию [185], при этом, если оно случается чаще одного раза в неделю, возрастает вероятность более длительной продолжительности дисменореи, увеличивается риск возникновения болезненных менструаций [158].
У мужчин с синдромом алкогольной зависимости наблюдается значительное снижение уровня тестостерона, объема семенной жидкости и концентрации сперматозоидов [186][187]. Среди бесплодных мужчин, принадлежащих к группе "ежедневно пьющих", качество спермы и гормональные характеристики значительно хуже по сравнению с другими группами [188]. Время до наступления беременности значительно дольше в парах, в которых партнер-мужчина употреблял более 20 единиц алкоголя еженедельно [189].
Питание. Потребление меньшего количества жиров, а также продуктов, богатых углеводами, клетчаткой, фолиевой кислотой и ликопином коррелирует с улучшением качества спермы и является более полезным для мужской фертильности [190][191]. При планировании рациона питания, способствующего улучшению параметров спермы, необходимо включение фруктов и овощей [192][193], бобовых [194] и рыбы [194][195] как источников антиоксидантов и полиненасыщенных жирных кислот (среди которых омега-3) и исключение таких продуктов, как переработанное мясо и жирные молочные продукты, являющихся источниками насыщенных жиров [195]. В целом, потребление фруктов и овощей показало устойчивую положительную связь с улучшением подвижности и морфологии [192][193]. Согласно шкале средиземноморской диеты, высокая приверженность этой диете тесно связана с лучшими параметрами спермы, то есть количеством, подвижностью и морфологией сперматозоидов [196], и более низким индексом фрагментации ДНК [197], чем у людей с более низкой приверженностью. Напротив, известно, что частое употребление красного мяса отрицательно связано с параметрами спермы [198]. Еще одной группой продуктов, оказывающих потенциально благоприятное влияние на мужскую фертильность, являются антиоксиданты (альбумин, церулоплазмин, ферритин, аскорбиновая кислота, α-токоферол, β-каротин, восстановленный глутатион, мочевая кислота и билирубин, а также ферменты супероксиддисмутаза, каталаза и глутатионпероксидаза), которые играют ключевую роль в организме, помогают удалить избыток активных форм кислорода в семенном эякуляте и способствуют их преобразованию в соединения, которые менее вредны для клеток [199]. У мужчин, принимающих пероральные антиоксиданты, наблюдается значительное увеличение частоты живорождения и увеличение частоты наступления беременности [200].
Особенности питания женщин также оказывают большое влияние на ее фертильность, особенно на овуляцию. Доказано, что замена углеводов животным белком вредна для овуляторной фертильности [201]. Добавление всего лишь одной порции мяса, особенно курицы или индейки, коррелирует с повышением на 32% вероятности развития овуляторного бесплодия [201]. Однако замена углеводов растительным белком обеспечивает защитный эффект [201]. Выбор трансжиров в рационе вместо мононенасыщенных жиров резко увеличивает риск овуляторного бесплодия [202]. Потребление трансжиров вместо углеводов коррелирует с увеличением риска нарушений овуляции на 73% [202]. Женщины, принимающие поливитамины, реже страдают овуляторным бесплодием [203]. Женщины, употребляющие продукты питания с более высоким содержанием мононенасыщенных жиров, растительных белков по сравнению с животным, сниженной гликемической нагрузкой и повышенным потреблением железа и поливитаминов, имели более низкие показатели бесплодия по причине нарушений овуляции [204].
Избыточная масса тела и ожирение. Известно негативное влияние избыточной массы тела и ожирения на женскую репродуктивную физиологию, проявляющееся нарушением менструального цикла, овуляции, патологией эндометрия и бесплодием [205][206]. Риск бесплодия в три раза выше у женщин с ожирением, чем у женщин без ожирения [207][208]. Ожирение влияет на фертильность, вызывая нарушение развития фолликулов яичников, качественные и количественные дефекты созревания ооцитов, а также приводит к аномальной предимплантации эмбриона [209]. При оценке связи между ожирением и выкидышем как при естественном, так и при вспомогательном зачатии, доказано, что риск выкидыша достигал примерно 40% у женщин с ожирением по сравнению с менее чем 15% у женщин с нормальным индексом массы тела [210]. Женщины с избыточным весом и ожирением имеют худшие результаты лечения бесплодия, плохо реагируют на индукцию овуляции, требуют более высоких доз гонадотропинов и более длительных курсов лечения для развития фолликулов и овуляторных циклов. Кроме того, выход ооцитов ниже у женщин с ожирением, что приводит к более высокой частоте отмены цикла [211]. Стимуляция яичников для вспомогательной репродукции приводит к образованию меньшего количества фолликулов и меньшего количества ооцитов, снижается уровень оплодотворения и качество эмбрионов, возрастает риск потери беременности на ранних сроках. Доказано, что потеря веса улучшает репродуктивные результаты за счет улучшения фертильности, а также за счет регуляризации менструальных циклов и увеличения вероятности спонтанной овуляции и зачатия у женщин с ановуляционным избыточным весом и ожирением. Потеря веса от 5 до 10% массы тела может определенно улучшить коэффициент фертильности [212], при этом потеря веса на 5% приводит к значительному улучшению эндокринных параметров, таких как снижение уровня свободного тестостерона, уровня ЛГ и инсулина с улучшением частоты овуляций [213]. Негативное влияние ожирения на фертильность у женщин может быть обратимым: у 90% женщин с ожирением, ранее имевших ановуляцию, при среднем снижении веса на 10 кг, начиналась овуляция [214].
Избыточная масса тела и ожирение являются важными факторами мужской фертильности [215]. У мужчин с ожирением в три раза чаще наблюдается снижение качества спермы, чем у мужчин с нормальным весом [216]. Несколько исследований показали, что увеличение индекса массы тела коррелирует со снижением концентрации сперматозоидов [217][218] и снижением подвижности сперматозоидов [219]. Также доказано, что у мужчин с избыточным весом наблюдается повышенное повреждение ДНК в сперматозоидах [220][221]. Существует связь между ожирением и эректильной дисфункцией, которая может быть следствием превращения андрогенов в эстрадиол [222]. За это преобразование отвечает фермент ароматаза, который обнаруживается преимущественно в жировой ткани [223]. По мере увеличения количества жировой ткани появляется больше ароматазы, доступной для преобразования андрогенов, и уровень эстрадиола в сыворотке увеличивается [220][224]. Ожирение также может влиять на другие гормоны, включая ингибин B и лептин. Сообщалось, что уровни ингибина B снижаются с увеличением веса, что приводит к снижению количества клеток Сертоли и выработки спермы [224], а уровень лептина, контролирующего в организме уровень аппетита, воспаление и снижение секреции инсулина, возрастает [225].
Женщины с низкой массой тела (индекс массы тела <18,5 кг/м2) также подвержены риску неблагоприятных исходов беременности и развития бесплодия. Хорошо известно, что женская репродуктивная функция чрезвычайно уязвима к энергетическому дисбалансу и изменениям в составе тела. Снижение доступности метаболического топлива ниже критического уровня из-за ограничения питания или увеличения расходов энергии соответствующим образом сопровождается активацией множественных нейроэндокринных изменений, что приводит к ановуляции и аменорее [226]. В частности, подкожный и абдоминальный жир, являющийся важнейшим резервуаром для хранения энергии в организме, оказывает значительное влияние на функцию яичников [227]. Преобразование андрогенов в эстрогены путем ароматизации происходит в жировой ткани; почти треть циркулирующих эстрогенов у женщин во время репродуктивной фазы происходит из этого преобразования. Жировая ткань влияет на направление метаболизма эстрогенов в более или менее мощные формы; более стройные женщины с пониженным количеством жира в организме показывают более высокие уровни менее мощных форм эстрогенов, таких как катехолэстрогены [227].
Низкая физическая активность (малоподвижный образ жизни). Мужчины, ведущие малоподвижный образ жизни, с большей вероятностью страдают от позднего мужского гипогонадизма, который вызван низким уровнем тестостерона, снижением либидо, эректильной дисфункцией и снижением жизнеспособности сперматозоидов [228]. Физически активные мужчины имеют большую долю подвижных сперматозоидов по сравнению с мужчинами, ведущими малоподвижный образ жизни, а умеренные физические нагрузки замедляют возрастные воспалительные процессы и повреждение ДНК в сперматозоидах [229]. Физические упражнения, повышая антиоксидантную защиту яичек, снижая уровень провоспалительных цитокинов и усиливая процесс стероидогенеза, приводят к улучшению сперматогенеза и качества спермы при бесплодии, вызванном образом жизни [230]. Вместе с тем тяжелый физические нагрузки у профессиональных спортсменов наоборот оказывают отрицательный эффект на мужскую репродуктивную систему. Доказано, что тренировки на выносливость среди велосипедистов вредны для морфологии сперматозоидов [231]. Езда на велосипеде более 5 ч в неделю имеет отрицательную корреляцию как с общим количеством подвижных сперматозоидов, так и с концентрацией сперматозоидов [232]. Кроме того, езда на велосипеде способствует повышению температуры в области мошонки, что оказывает негативное влияние на сперматогенез [233]. В настоящее время хорошо известно, что сидячая рабочая поза также связана с повышенной температурой мошонки. У мужчин, сидящих на работе в течение 8 ч в день, температура мошонки в среднем повышается на 0,7°C в течение дня по сравнению с работниками, находящимися в сидячем положении тела менее 8 ч, что также негативным образом сказывается на процессе сперматогенеза [234].
Умеренная физическая активность оказывает положительное воздействие на фертильность в сочетании со снижением веса у женщин с ожирением [214]. Вместе с тем чрезмерные физические нагрузки, при которых меняется энергетический баланс (потребность в энергии превышает ее потребление), могут негативно повлиять на репродуктивную систему [235], привести к дисфункции гипоталамуса и изменениям уровня гонадотропин-рилизинг-гормона, нарушениям менструального цикла, особенно среди спортсменок [236]. Доказано, что повышенная частота, интенсивность и продолжительность физических упражнений значительно коррелируют со снижением фертильности у женщин, увеличивая риск развития бесплодия у женщин, которые тренировались каждый день [237]. Широкий спектр менструальных дисфункций — от задержки менструаций до дефицита лютеиновой фазы, олигоменореи, ановуляции и аменореи, связан со спортивной деятельностью женщин [238-240]. Распространенность аменореи, вызванной физической нагрузкой, варьируется от 5-20% у активно тренирующихся женщин до 40-50% у профессиональных спортсменок [241][242].
Малоподвижный образ жизни также в известной мере влияет на исходы беременности и родов [243], оказывая положительную связь с секрецией лептина [244], который может снижать фертильность и вызывать бесплодие.
Психоэмоциональный стресс. Связь между мужским бесплодием и психологическим стрессом является спорной, поскольку данные противоречивы. Профессиональный стресс, связанный с работой, определенные жизненные события, социальное напряжение и эмоциональное выгорание могут оказывать существенное негативное влияние на качество спермы и приводить к мужскому бесплодию [245-247]. Анализы спермы студентов-медиков во время экзаменационных периодов [248][249] и мужчин, переживших войну [250-252], периоды стресса на работе [253] и недавнюю тяжелую утрату [254], показали снижение концентрации сперматозоидов. Само лечение бесплодия может также стать для мужчины стрессом. Пара, у которой не удалось забеременеть, может испытывать чувство разочарования и эмоционального потрясения [255] из-за длительных усилий с точки зрения приема лекарств, стоимости и времени лечения. Влияние психологического стресса на эректильную функцию является хорошо известным клиническим феноменом. Как острый, так и хронический психологический стресс может привести к эректильной дисфункции [256]. Пары, испытывающие проблемы с фертильностью, часто вступают в половой акт по расписанию в период овуляции. Этот строгий график может быть весьма стрессовым для мужчин и может привести к тревоге и разочарованию, потенциально вызывая эректильную и эякуляторную дисфункцию [257]. Аналогичным образом, посттравматическое стрессовое расстройство (длительное состояние, возникающее после воздействия опасного для жизни события) может привести к сексуальной дисфункции (включая эректильную дисфункцию и проблемы с эякуляцией), а также иных симптомов, включая навязчивые воспоминания, состояние гипервозбуждения. и избегание раздражителей [258]. Психологический стресс уже давно считается возможным фактором, способствующим развитию хронического простатита/синдрома хронической тазовой боли, а также его обострению [259][260].
Как в общей популяции женщин, так и среди женщин, страдающих бесплодием, психологический стресс достоверно связан со снижением показателей зачатия и продолжительностью менструальных циклов (≥35 дней), а также с более низкими показателями репродуктивного здоровья, включающими количество ооцитов, возможность оплодотворения и наступления беременности, частотой живорождения [261-265]. Кроме того, у бесплодных женщин были выявлены "хронические" психосоциальные стрессоры, повышающие вероятность снижения овариального резерва [266].
Депрессия, избегание или избыточное выражение эмоций могут иметь одинаковые последствия для женской плодовитости [264]. Депрессия значимо коррелирует с альтернативным проявлением стресса, т.е. тревогой, влияющей на высвобождение кортизола [267], и такие симптомы наблюдаются примерно у 37% бесплодных женщин [268]. Соответственно, обе эмоции преобладают у женщин-партнеров бесплодных пар [269] и более распространены среди женщин, страдающих бесплодием, по сравнению с фертильными женщинами [270-272]. Роль эмоционального стресса и тревоги до сих пор непонятна, но небольшое количество данных свидетельствует о том, что индукция окислительного стресса может быть механизмом, с помощью которого психосоциальные стрессоры влияют на качество ооцитов через ухудшение общего здоровья женщины [273][274].
Нарушение сна. Определенные физиологические периоды жизни, характеризующиеся своеобразной гормональной секрецией (например, беременность, лактация и менопауза) или патологическими состояниями (например, синдром поликистозных яичников), часто связаны с нарушениями сна [275][276]. Однако продемонстрирована и обратная связь: известно, что нарушения сна у женщин приводят к нарушениям менструального цикла [277]. Доказано, что низкая продолжительность сна может оказывать негативное влияние на менструальную цикличность, увеличивая частоту ее нарушений при продолжительности сна менее 5 ч [279]. Некоторые данные указывают на прямую корреляцию между качеством сна и высокой частотой нарушений овариального цикла [280][281]. Снижение качества сна предлагается рассматривать в качестве фактора риска снижения овариального резерва. У женщин вечернего хронотипа может наблюдаться более продолжительный менструальный цикл [282]. Доступны более надежные данные относительно посменной работы, которая приводила к нарушению менструального цикла [283-285], при этом любой вид посменной работы был связан с более высоким риском нарушения продолжительности овариального цикла [286].
Связь между сном и статусом мужской фертильности в основном основана на анализе спермы. В отдельных исследованиях отмечается, что параметры спермы хуже у мужчин, которые поздно отходят ко сну и мало спят [287-289]. У мужчин с вечерним хронотипом отмечается худший репродуктивный профиль [287][289]. Отдельные исследования показали, что у мужчин с посменной работой чаще встречаются случаи олигозооспермии [290][291]. Нарушение сна связано с повышенным риском снижения количества и концентрации сперматозоидов, а также более низкой долей сперматозоидов с нормальной морфологией по сравнению с показателями, отмечающимися при нормальном сне [292].
ЦЕЛЬ
Повысить приверженность работодателей к реализации мероприятий, направленных на укрепление здоровья работающих2, и мотивировать работников вести здоровый образ жизни.
ОПИСАНИЕ
Реализация подпрограммы не требует дополнительного финансирования.
Для реализации подпрограммы необходимо руководствоваться рекомендациями "Корпоративные модельные программы "Укрепление здоровья работающих" 3.
ОТВЕТСТВЕННЫЕ
— руководитель кадровой службы организации (менеджер по персоналу);
— руководитель регионального Центра общественного здоровья и медицинской профилактики.
СРОКИ РЕАЛИЗАЦИИ
Постоянно, с ежегодным контролем эффективности выполняемых мероприятий, а также согласно рекомендациям "Корпоративные модельные программы "Укрепление здоровья работающих"3 с учетом специфики реализуемых мероприятий.
ИНДИКАТОРЫ РЕЗУЛЬТАТА
По каждому направлению и мероприятию представлены в соответствующих разделах рекомендаций "Корпоративные модельные программы "Укрепление здоровья работающих"3.
1.6. ПОДПРОГРАММА "КОМПЛЕКСНАЯ ПОДДЕРЖКА В ПЕРИОДЫ НАСТУПЛЕНИЯ МЕНОПАУЗЫ У ЖЕНЩИН И АНДРОПАУЗЫ У МУЖЧИН"
АКТУАЛЬНОСТЬ
Менопауза является естественным процессом репродуктивного старения, проявляющимся окончательным прекращением функции яичников и выработки репродуктивных гормонов, а также необратимой потерей фертильности. Средний возраст наступления менопаузы составляет примерно 48-52 года [293], "ранняя менопауза" определяется как наступающая в возрасте от 40 до 45 лет, а полная потеря функции яичников в возрасте до 40 лет называется преждевременной. С развитием менопаузы ассоциировано также развитие сопутствующих патологических состояний и заболеваний:
— нарушение сна [294-296], расстройства настроения, такие как депрессия и тревога [297], боль в мышцах и суставах [298];
— развитие урогенитальной атрофии (сухость влагалища, болезненность полового акта (диспареунию), зуд вульвы, жжение и дискомфорт, а также рецидивирующие урогенитальные инфекции) [299]. Симптомы урогенитальной атрофии сохраняются на протяжении всей жизни в постменопаузе и могут оказывать серьезное влияние на сексуальное здоровье и качество жизни [300]. Боль во время полового акта, вторичная по отношению к вульвовагинальной атрофии, приводит к снижению сексуального влечения, проблемам в отношениях и снижению физического и эмоционального сексуального удовлетворения [301];
— остеопороз — чем раньше наступает менопауза, тем выше риск остеопороза в более позднем возрасте [302];
— метаболические последствия. Распространенность ожирения выше у женщин в постменопаузе, чем у женщин в пременопаузе [303]. Абдоминальное ожирение и снижение уровня эстрогена в менопаузе связаны с неблагоприятными метаболическими изменениями, такими как резистентность к инсулину, склонность к развитию сахарного диабета 2 типа и дислипидемия, характеризующаяся высокими уровнями триглицеридов;
— сердечно-сосудистые заболевания. Вследствие дефицита эстрогена после менопаузы у женщин возрастает риск развития атеросклеротических процессов, ишемической болезни сердца [304], повышения артериального давления [305]. Риск инсульта удваивается в течение первого десятилетия после менопаузы и в конечном итоге превышает риск инсульта у мужчин старшего возраста [306];
— когнитивные нарушения. Менопауза влияет на когнитивные функции, в частности, на аспекты, связанные с вербальной памятью и беглостью речи [307].
Андропауза не рассматривается как эквивалент менопаузы в связи с тем, что у мужчин не происходит внезапной остановки функций половых желез, снижение уровня тестостерона, подвижности сперматозоидов, а также эндо- и экзокринной функций яичек происходит постепенно, а фертильность сохраняется до глубокой старости [308]. Некоторыми исследователями процесс наступления андропаузы определяется с момента начала снижения уровня тестостерона примерно на 1% в год после 30 лет [309]. При сравнении мужчин в возрасте до 30 лет с мужчинами в возрасте 50 лет и старше большинство исследований документально подтверждают снижение объема спермы на 20-30% между двумя группами [310], а также подвижности сперматозоидов на 3-37% [311][312]. Наступление андропаузы сопровождается постепенным снижением почти всех физиологических функций, что клинически отражается в:
— ухудшении общего самочувствия, бессоннице, раздражительности, повышенном потоотделении;
— уменьшении мышечной массы, силы и энергии, развитии абдоминального ожирения. Существует значительная корреляция между мышечной массой и уровнем свободного тестостерона [313][314]. Изменения в составе тела у пожилых мужчин не являются единственным следствием снижения уровня тестостерона, определяясь также возрастным снижением уровня гормона роста (соматопауза) и естественным снижением физической активности [307];
— снижении мужественности, степени оволосения по мужскому типу, либидо и сексуальной активности;
— повышении частоты эректильной дисфункции резко возрастает с возрастом от 8% в возрасте 55 лет до более 50% в возрасте 75 лет [315]. Сахарный диабет является частой причиной ранней импотенции и гиперпролактинемии. И сахарный диабет, и гиперпролактинемия часто сопровождаются гипотестостеронемией. Часто причиной импотенции могут быть и такие лекарства, как антигипертензивные средства (бета-блокаторы, ингибиторы ангиотензинпревращающего фермента), трициклические фенотиазины, бензодиазепины [316];
— развитии атеросклероза и коронарного стеноза. Существует обратная корреляция между уровнями тестостерона и атерогенным липидным профилем [317], атеросклерозом или степенью коронарного стеноза соответственно [318], тогда как прием андрогенов в физиологических пределах нормализует липидный профиль у пожилых мужчин, вероятно, за счет повышения чувствительности к инсулину [319]. Более того, тестостерон снижает уровень холестерина [320], оказывает прямое воздействие на кровеносные сосуды [321], на свертывание крови [322] и на фибринолиз [323].
— снижении когнитивных функций, пространственной ориентации и забывчивости. Прогрессивное снижение секреции тестостерона у стареющих мужчин способствует избирательным потерям памяти и когнитивных функций [324].
ЦЕЛЬ
Обеспечить возможностями психологической и медицинской поддержки работающих женщин и мужчин, у которых в связи с возрастными изменениями отмечается развитие симптомов, характерных для менопаузы и андропаузы.
ОПИСАНИЕ
При реализации подпрограммы в организации рекомендуется:
1) Провести анкетирования женщин (прежде всего, в возрасте старше 45 лет) по шкале Грина (Приложение 1) и мужчин (прежде всего в возрасте старше 55 лет) по шкале AMS (Приложение 2) для определения симптомов, характерных для менопаузы и андрогенного дефицита соответственно.
2) Обеспечить взаимодействие с региональным центром общественного здоровья и медицинской профилактики с привлечением врачей-специалистов (врач-психотерапевт, врач-эндокринолог, врач-акушер-гинеколог (при необходимости), врач-
уролог (при необходимости)) для проведения информационной кампанию среди работников организации (прежде всего для женщин в возрасте старше 45 лет и мужчин в возрасте старше 55 лет) о возрастных симптомах менопаузы и андропаузы и тактике поведения при их наличии.
3) Создать возможность для работников организации для посещения медицинской организации и консультации у профильного врача-специалиста (врач-эндокринолог, врач-уролог (при необходимости), врач-акушер-гинеколог (при необходимости)).
4) Обеспечить работникам полную или частичную оплату лекарственных препаратов, выписанных для проведения заместительной гормональной терапии (ЗГТ).
5) Создать оптимальные условия на рабочем месте, учитывающие индивидуальные психологические особенности, характерные для работников, имеющих симптомы менопаузы и андропаузы соответственно.
Реализация подпрограммы может потребовать дополнительного финансирования для оплаты лекарственных препаратов, выписанных для проведения ЗГТ.
Для реализации подпрограммы необходимо:
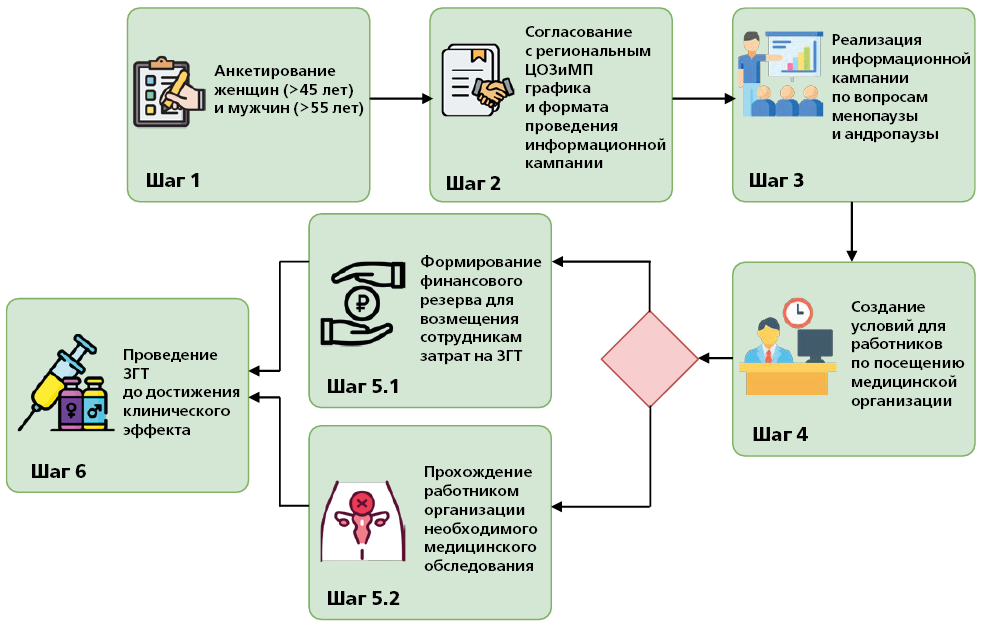
ОТВЕТСТВЕННЫЕ
— руководитель кадровой службы организации (менеджер по персоналу);
— руководитель регионального Центра общественного здоровья и медицинской профилактики;
— руководитель медицинской организации, в которой работнику проводится ЗГТ.
СРОКИ РЕАЛИЗАЦИИ
Для информационной кампании — регулярно, не реже 1 раза в год для целевой группы работников (прежде всего для женщин в возрасте старше 45 лет и мужчин в возрасте старше 55 лет)
Для проведения ЗГТ — в зависимости от медицинских показаний и клинической эффективности.
ИНДИКАТОРЫ РЕЗУЛЬТАТА
Для работодателя и организации:
- Доля работников организации (женщин в возрасте старше 45 лет и мужчин в возрасте старше 55 лет), прошедших анкетирование по шкале Грина и шкале AMS, от всех работников организации данных возрастных групп. Рекомендуется, чтобы данный показатель составлял не менее 85% как для женщин, так и для мужчин.
- Доля работников организации (женщин в возрасте старше 45 лет и мужчин в возрасте старше 55 лет) от всех работников организации данных возрастных групп, принявших участие в информационной кампании. Рекомендуется, чтобы данный показатель составлял не менее 85% как для женщин, так и для мужчин.
- Доля работников организации (женщин в возрасте старше 45 лет и мужчин в возрасте старше 55 лет), которым за счет работодателя проводится полное или частичное возмещение затрат на приобретение лекарственных препаратов для ЗГТ, от всех работников организации, нуждающихся в ЗГТ. Рекомендуется, чтобы данный показатель составлял не менее 85% как для женщин, так и для мужчин.
Для системы здравоохранения:
- Доля работников организации, которым назначена ЗГТ, от всех работников организации, которым необходима ЗГТ. Рекомендуется, чтобы данный показатель составлял не менее 85%.
- Доля работников организации, у которых достигнута клиническая эффективность от ЗГТ. Рекомендуется, чтобы данный показатель составлял не менее 85% как для женщин, так и для мужчин.
1.7. ПОДПРОГРАММА "ЗАБОТА О СЕМЬЕ"
АКТУАЛЬНОСТЬ
Для формирования у молодых людей положительного восприятия семейных ценностей и настроя на создание семьи, на рабочем месте должны быть созданы соответствующие условия и реализованы мероприятия, предусматривающие возможность проведения психологического консультирования по вопросам материнства и отцовства, психологическую поддержку работников после рождения детей, социальную поддержку работников в отношении изменения условий труда и создания возможностей для трудовой мобильности, а также расширение набора социальных услуг, оказываемых за счет работодателя, финансового стимулирования работников за рождение детей, создания возможностей для организации на рабочем месте совместного времяпрепровождения родителей-работников организации и их детей.
Психологические аспекты отцовства. Тревога и депрессия — две наиболее распространенные проблемы психического здоровья, с которыми сталкиваются отцы в перинатальный период [325-328]. Уровень распространенности тревожного расстройства у мужчин колеблется от 4,1 до 16% во время беременности их партнерши и от 2,4 до 18% в послеродовой период [326], а уровень распространенности дородовой и послеродовой депрессии у отцов колебался от 1,2 до 25,5% [329]. В период между первым триместром беременности и годом после родов депрессия выявлялась у 10,4% отцов, при этом пиковый период приходился на период от трех до шести месяцев после родов, что аналогично результатам для женщин в послеродовом периоде [325]. Беременность является наиболее сложным периодом для психологической реорганизации личности отца, а роды — наиболее эмоциональными моментами, включающими смешанные чувства, варьирующиеся от беспомощности и тревоги до удовольствия и гордости [330]. Однако послеродовой период в течение первого года после рождения ребенка был самым трудным периодом, поскольку отцам приходилось сбалансировать различные требования, предъявляемые к ним, включая личные рабочие потребности, их новую роль в качестве родителя, эмоциональные и реляционные потребности семьи, а также социальное и экономическое давление [321]. Основными факторами, которые способствуют стрессу у отцов в перинатальном периоде, являются негативные переживания по поводу беременности, ролевые ограничения, связанные с отцовством, страх перед родами и чувство некомпетентности в уходе за ребенком [327].
Психологические аспекты материнства. Переход к материнству отмечен гормональными колебаниями (снижение уровня эстрогена и прогестерона после родов) [330], лишением сна и адаптацией к новой роли, что потенциально влияет на психическое благополучие женщины. Послеродовые расстройства настроения могут включать послеродовую депрессию, тревожные расстройства и даже редкие, но тяжелые случаи послеродового психоза [331]. Послеродовая депрессия поражает около 10-20% молодых матерей во всем мире [332] и характеризуется стойкой грустью, безнадежностью и потерей интереса или удовольствия от занятий, которые ранее приносили удовольствие. Она часто проявляется в течение первых нескольких недель после родов, но может проявиться и через год. Физические симптомы, такие как изменения аппетита и режима сна, могут сопровождать эмоциональный стресс [333]. Послеродовые тревожные расстройства охватывают ряд состояний, связанных с тревогой, включая генерализованное тревожное расстройство, паническое расстройство и обсессивно-компульсивное расстройство. Молодые матери с послеродовой тревогой могут испытывать чрезмерное беспокойство, беспокойство и навязчивые мысли о безопасности своего ребенка [334]. Послеродовой психоз относительно редок, представляет собой тяжелое расстройство, характеризующееся галлюцинациями, бредом и дезорганизованным мышлением. Обычно появляется в течение первых нескольких недель после родов и требует немедленного медицинского вмешательства [335].
Социальная поддержка работников. Рождение ребенка и возвращение на работу после декретного отпуска является переходным этапом, во время которого женщина оказывается в состоянии перестройки своей жизни с точки зрения необходимости соблюдения баланса между работой и материнством [336]. Отношение к соблюдению женщинами баланса на работе имеет очевидное намерение, чтобы рабочая нагрузка не сказывалась на вопросах материнства, и на рабочем месте создавались более гибкие условия для реинтеграции в трудовой процесс [337]. Одним из способов ответственного поведения матери, стремящейся справиться с рабочей нагрузкой, может быть сокращение рабочего времени [338]. Вместе с тем сокращение рабочего времени и статуса на рабочем месте могут являться факторами, оказывающими негативное влияние на чувство благополучия сотрудников [339] и психическое здоровье женщин [340]. Выявление общих тенденций дает работодателям возможность совершенствовать подходы к нормированию труда, развивать определенную трудовую культуру на рабочем месте, соотносить требования работы с возможностями сотрудников, а также оказывать поддержку работающим матерям в обеспечении баланса между работой и семейной жизнью [341].
Финансовое стимулирование работников. Немаловажными факторами, влияющими на решение молодых семей иметь детей, являются стабильный финансовый доход и наличие гарантированного рабочего места [342], экономической и социальной независимости [343, 344], доступ к качественному жилью и ипотечным кредитам на обеспечение жильем [345]. Одним из важнейших элементов, который в различных исследованиях выделен как фундаментальный, определяющих склонность пар к родительству, является экономический статус или уровень дохода семьи. Опасения по поводу будущих экономических условий и экономического статуса страны являются одними из наиболее важных причин нежелания быть родителями [346]. Превентивные причины воздержания от родительских обязанностей включают опасения по поводу будущего образования, условий трудоустройства, экономических проблем, связанных с воспитанием новых детей, и недостаточного дохода [347]. Кроме того, финансовые затраты на рождение детей имеют значительную и отрицательную корреляцию с желаемой рождаемостью, учитывая потерю дохода женщин, которые делают выбор в пользу материнства [348].
Совместное времяпрепровождение родителей и детей. Для работающих матерей с маленькими детьми особую роль играет возможность создания на рабочем месте условий для грудного вскармливания [349]. Работающим матерям часто бывает трудно продолжать грудное вскармливание на работе из-за отсутствия поддержки грудного вскармливания на рабочем месте [350]. Вынужденный сокращенный отпуск по беременности и родам, проблемы со временем и местом, работа полный рабочий день, недостаточные перерывы в течение рабочего дня, отсутствие поддержки со стороны руководства организации, негативная реакция со стороны коллег, отсутствие письменных правил, регулирующих и поддерживающих грудное вскармливание на рабочем месте, отсутствие конфиденциальности и неспособность матери найти время и место для сцеживания молока являются одними из препятствий на пути продолжения грудного вскармливания у работающих женщин [351]. Грудное вскармливание также представляет огромное значение для общественного здравоохранения, поскольку оно связано с улучшением показателей здоровья матерей и младенцев, включая снижение уровня различных инфекций среди младенцев и снижение риска ожирения для детей и матерей [352][353].
Время, проведенное с родителями, является важным фактором здоровья и развития детей. Совместная деятельность способствует близким, заботливым отношениям, которые имеют решающее значение для психологической и поведенческой адаптации детей [354-356], а также для их способности развивать близкие отношения со сверстниками [357]. Совместное времяпровождение между родителями и детьми также дает родителям возможность следить за деятельностью своих детей и предотвращать поведение, связанное с риском для здоровья [358], пропагандировать здоровое питание и физические упражнения [359][360], организовывать своевременные визиты к врачу [361, 362], развивать важные навыки и знания.
Органичная реинтеграция матерей в рабочую среду также является важнейшей задачей для сохранения репродуктивного здоровья и желания для дальнейшего деторождения. На рабочем месте матери зачастую сталкиваются с так называемым "наказанием за материнство", когда их считают непригодными для руководящих должностей, оценивают как менее компетентных и менее преданных своей карьере, они получают более низкую зарплату и лишаются возможности карьерного роста [363]. Материнство также вынуждает женщин отказываться от прежней работы из-за необходимости ухода за детьми и соблюдения баланса между работой и личной жизнью [364]. В некоторых случаях возникают вынужденные перерывы в карьере, когда женщины возвращаются на работу позже, чем ожидалось, прибегая к неформальной, гибкой работе или работе с частичной занятостью, откладывая возможности продвижения по службе или даже бросая работу на неопределенный срок [365, 366].
ЦЕЛЬ
Создать на рабочем месте условия, благоприятствующие созданию и сохранению крепкой семьи за счет реализуемого работодателем комплекса мер психологической поддержки, социального и материального стимулирования, а также организационно-планировочных решений, направленных на обеспечение комфортного времяпрепровождения родителей-работников организации с их детьми.
ОПИСАНИЕ
При реализации подпрограммы в организации рекомендуется:
1) Совместно с региональным центром общественного здоровья и медицинской профилактики с привлечением соответствующих врачей-специалистов провести для работников ряд тематических мероприятий: школы (семинары) для беременных, школы (семинары) по подготовки к беременности и родам, психологическое консультирование по вопросам материнства и отцовства.
2) Разработать стандарт трудовых функций, выполняемых сотрудницей женского пола в период беременности и после родов, исходя из специфики деятельности организации и с учетом необходимости более низкой нагрузки и интенсивности в рамках трудового процесса.
3) Обеспечить гибкие условия труда и возможность гибридного формата работы для сотрудниц женского пола в период беременности и после родов.
4) Предусмотреть возможность выплаты пособия от работодателя за рождение ребенка и различные варианты материальной помощи.
5) Предусмотреть возможность создания в организации комнаты для грудного вскармливания, комнат для ухода за ребенком, игровых комнат для детей сотрудников.
6) Предусмотреть возможность создания специального социального пакета для сотрудников, включающего предоставление различных услуг для детей (путевки в оздоровительный лагерь, посещение творческих кружков и спортивных секций и т.д.).
7) Разработать программу трудовой реинтеграции родивших сотрудниц, вышедших на работу после отпуска по уходу за ребенком.
Реализация подпрограммы может потребовать дополнительного финансирования за счет средств работодателя на выплаты пособий и материальной помощи, расширение социального пакета, создание комнат для совместного времяпрепровождения сотрудников организации с их детьми.
Для реализации подпрограммы необходимо:
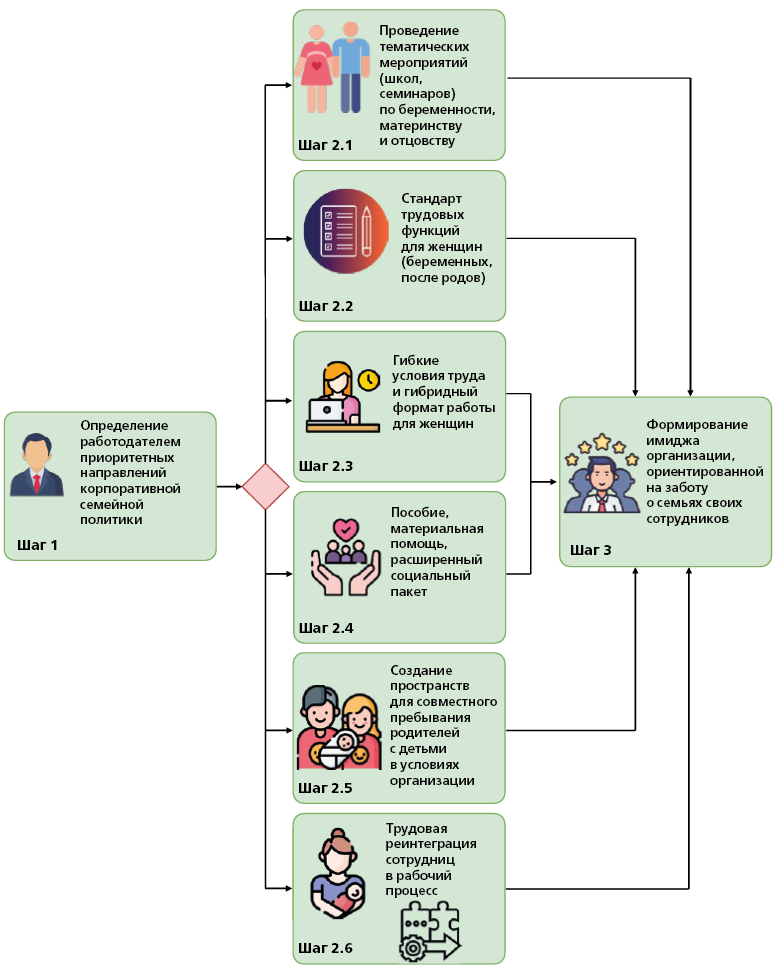
ОТВЕТСТВЕННЫЕ
— руководитель организации;
— руководитель кадровой службы организации (менеджер по персоналу);
— руководитель регионального Центра общественного здоровья и медицинской профилактики
СРОКИ РЕАЛИЗАЦИИ
На регулярной основе, в зависимости от характера реализуемых мероприятий и результатов оценки их эффективности (целесообразности).
ИНДИКАТОРЫ РЕЗУЛЬТАТА
Для работодателя и организации рекомендуется проведение оценки по следующим вопросам:
1) Реализуются ли для сотрудников организации тематические мероприятия по вопросам подготовки к беременности и родам, материнства и отцовства (ДА/НЕТ).
2) Разработан ли в организации стандарт или иной документ, регламентирующий трудовые функции, выполняемые сотрудницами женского пола в период беременности и после родов (ДА/НЕТ).
3) Имеются ли в организации гибкие условия труда и возможность гибридного формата работы для сотрудниц женского пола в период беременности и после родов (ДА/НЕТ).
4) Проводятся ли работодателем выплаты пособия за рождение ребенка и (или) имеются иные варианты материальной помощи (ДА/НЕТ).
5) Имеется ли в организации комната для грудного вскармливания и (или) комната для ухода за ребенком и (или) игровая комната для детей сотрудников (ДА/НЕТ).
6) Предоставляет ли работодатель для сотрудников расширенный социальный пакет (ДА/НЕТ).
7) Имеется ли в организации программа (порядок, практика, положение и т.д.) трудовой реинтеграции родивших сотрудниц, вышедших на работу после отпуска по уходу за ребенком (ДА/НЕТ).
Если в организации не менее 2 индикаторов результата имеют положительную оценку, то реализация программы "Забота о семье" может характеризоваться, как "удовлетворительная", если не менее 4 индикаторов — "хорошая", не менее 5 индикаторов — "отличная".
ЗАКЛЮЧИТЕЛЬНЫЕ ПОЛОЖЕНИЯ ПОДПРОГРАММ
При планировании и реализации в организации отдельных подпрограмм, направленных на сохранение и укрепление репродуктивного здоровья ее работников, ответственным исполнителям рекомендуется учитывать возможность проведения иных мероприятий, не обозначенных в указанных подпрограммах, а также не ограничиваться рамками отдельно взятой подпрограммы, принимая во внимание те мероприятия, которые по сути и содержанию взаимоувязаны друг с другом в нескольких подпрограммах, изложенных в настоящих методических рекомендациях.
Примеры лучших практик реализации отдельных мероприятий или подпрограмм, указанных в настоящих методических рекомендациях, представлены в Приложениях 3 (российские практики) и 4 (зарубежные практики).
Приложение 1
Оценка тяжести климактерического синдрома по шкале Грина
Симптомы | нет симптома | слабое | умеренное проявление симптома | тяжелое проявление симптома |
1. Быстрое или сильное сердцебиение | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
2. Чувство напряженности, нервозности | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
3. Нарушения сна | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
4. Возбудимость | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
5. Приступы тревоги, паники | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
6. Трудности в концентрации внимания | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
7. Чувство усталости или недостатка энергии | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
8. Потеря интереса ко многим вещам | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
9. Чувство недовольства или депрессия | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
10. Плаксивость | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
11. Раздражительность | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
12. Чувство головокружения или обморок | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
13. Давление или напряжение в голове, теле | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
14. Чувство онемения и дрожь в различных частях тела | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
15. Головные боли | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
16. Мышечные и суставные боли | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
17. Слабость в руках или ногах | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
18. Затрудненное дыхание | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
19. Приливы | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
20. Ночная потливость | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
21. Потеря интереса к сексу | 0 ☐ | 1 ☐ | 2 ☐ | 3 ☐ |
Общая сумма баллов по Опроснику: |
Пояснение: необходимо выбрать в каждой строке один вариант ответа, наиболее подходящий состоянию на момент осмотра и поставить рядом с ним знак V или X в окошке. После чего, проводится подсчет суммы баллов.
Степень выраженности климактерического синдрома по результатам тестирования:
- 1-11 баллов — слабая.
- 12-19 баллов — средняя.
- 20 баллов и выше — тяжелая.
Приложение 2
AMS (aging male symptoms) опросник симптомов старения мужчины
Какие из симптомов наблюдаются у Вас в настоящее время? | ||||||
Симптомы | нет 1 | слабые 2 | умеренные 3 | выраженные 4 | очень выраженные 5 | |
1 | Ухудшение самочувствия и общего состояния | |||||
2 | Боли в суставах и мышечные боли (боли в нижней части спины, боли в суставах, боли в пояснице, боли по всей спине) | |||||
3. | Повышенная потливость (неожиданные/внезапные периоды повышенного потоотделения, приливы жара, независимые от степени напряжения) | |||||
4. | Проблемы со сном (трудности с засыпанием, на протяжении сна, ранним пробуждением, | |||||
5. | Повышенная потребность в сне, частое ощущение усталости | |||||
6. | Раздражительность (ощущения агрессивности, раздражения по пустякам, уныние) | |||||
7 | Нервозность (внутреннее напряжение, суетливость, беспокойство) | |||||
8. | Тревожность (приступы паники) | |||||
9. | Физическое истощение/упадок жизненных сил, общее снижение работоспособности, пониженная активность, отсутствие интереса к занятиям досуга, сниженная самооценка, неудовлетворенность сделанным, достигнутым, необходимость заставлять себя проявлять активность | |||||
10. | Снижение мышечной силы (ощущение слабости) | |||||
11. | Депрессия (чувство подавленности, грусти, слезливость отсутствие стимулов, колебания в настроении; | |||||
12. | Ощущение, что жизненный пик пройден | |||||
13. | Опустошенность, ощущение "дошел до ручки" | |||||
14. | Уменьшение роста бороды | |||||
15. | Снижение способности и частоты сексуальных отношений | |||||
16. | Снижение количества утренних эрекций | |||||
17. | Снижение сексуального желания/либидо отсутствие желания сексуальных контактов) | |||||
Наблюдаете ли Вы у себя какие-либо другие заметные симптомы? Если "да", опишите: | да | нет | ||||
Оценка результатов анкетирования по опроснику AMS:
- 17-26 баллов — симптомы андрогенного дефицита не выражены.
- 27-36 баллов — симптомы андрогенного дефицита слабо выражены.
- 37-49 баллов — симптомы андрогенного дефицита средней выраженности.
- >50 баллов — симптомы андрогенного дефицита резко выражены.
Приложение 3
ПРИМЕРЫ РОССИЙСКИХ ПРАКТИК РЕАЛИЗАЦИИ КОРПОРАТИВНЫХ ПРОГРАММ ИЛИ ОТДЕЛЬНЫХ МЕРОПРИЯТИЙ, НАПРАВЛЕННЫХ НА СОХРАНЕНИЕ И УКРЕПЛЕНИЕ РЕПРОДУКТИВНОГО ЗДОРОВЬЯ
По подпрограмме "Оценка репродуктивного здоровья для создания семьи"
 | Управляющая компания "Металлоинвест" реализует проект "Женское здоровье", направленный на совершенствование комплексной системы ранней диагностики и профилактики заболеваемости рака молочной железы. |
 | Центр общественного здоровья и медицинской профилактики ОГАУЗ "Смоленский областной врачебно-физкультурный диспансер" на официальном сайте размещает информацию о репродуктивном здоровье и беременности (памятка для пациентов, планирующих беременность; курение и беременность: как сигареты влияют на зачатие; как подготовиться к исследованиям у гинеколога; как улучшить показатели спермограммы; правила подготовки к беременности; репродуктивное здоровье мужчины и др.). Информация тиражируется для работодателей Смоленской области. |
По подпрограмме "Повышение грамотности в вопросах
полового воспитания и поведения"
Примером организационного решения, направленного на информирование работников по вопросам профилактики ЗППП, в том числе ВИЧ/СПИД, может являться опыт муниципального казенного предприятия муниципального образования города Тула "Тулгорэлектротранс" (1 257 работников, ID 1702009621 4 от 10 апреля 2024 г.), которые 19 мая 2023 г. приняли участие в мероприятии "Профилактика ВИЧ/СПИД на рабочих местах". Целью мероприятия являлось проведение информационно-разъяснительной работы по вопросам профилактики ВИЧ/СПИД на рабочих местах. Для этого:
— размещена информация на информационных стендах профсоюзных уголках в управлении, в службе автобусного транспорта, в троллейбусном депо, в трамвайном депо;
— размещен материал на интернет-сайте МКП "Тулгорэлектротранс";
— проведено индивидуальное информирование сотрудников, в том числе при приеме на работу (ознакомление с информацией в профкоме, при проведении инструктажей по охране труда);
— проведено информирование в медпунктах предприятия.
По подпрограмме "Репродуктивное здоровье без факторов риска
хронических неинфекционных заболеваний"
 | ПАО "Энел Россия" Программа "Стресс.0" — проект, направленный на определение факторов стресса и разработку возможных мер по его снижению. Уровень стресса и его причины были выявлены с помощью проведения опроса среди всех сотрудников компании. Опрос состоял из 8 разделов, в каждом из которых вопросы разбиты на подразделы. Результаты были консолидированы как в общем по стране, так и в разбивке по филиалам. Далее были выделены проблемные зоны и обозначен план мероприятий по минимизации уровня стресса. Например, для повышения кросс-функционального взаимодействия в компании существует проект E-cross (кросс-функциональная ротация в формате двухдневной стажировки или четырехчасового мастер-класса). Также проводится дополнительное обучение (как внутреннее, так и внешнее) по управлению стрессом и энергией. Мероприятия проводятся регулярно в течение всего года. |
 | ООО "Сахалинская Энергия" реализует программу "Здоровье на рабочем месте". Для работников компании, осуществляющих деятельность во вредных, опасных и тяжелых условиях труда, проводятся периодические медицинские осмотры, для офисных работников организована диспансеризация работников компании. При выявлении отклонений в состоянии здоровья назначаются лечебно-оздоровительные мероприятия. Компания уделяет особое внимание предотвращению появления усталости у сотрудников. В связи с этим разрабатываются и внедряются меры для оценки риска. В оценку риска включаются в т.ч. длительность рабочего дня, рабочей смены, максимальная продолжительность вахты, чередование ночной и дневной смены. Персонал компании имеет доступ к интерактивным информационным материалам об управлении рисками, связанными с усталостью. Помимо обязательных программ охраны здоровья компания проводит политику поощрения персонала к поддержанию хорошей физической формы и профилактике заболеваний. |
 | ООО "Газпром добыча Оренбург" В компании с 2003 г. разработана и действует целевая программа "Здоровый образ жизни работников". Главной стратегической целью программы является улучшение здоровья работников компании (в частности, отказ от курения), повышение мотивации к формированию потребности в здоровом образе жизни и физической активности. В этих целях: • проводятся медико-социологические исследования для выявления распространенности поведенческих факторов риска и профессионального стресса; • создана постоянно действующая информационно-пропагандистская система, направленная на повышение уровня знаний работников о влиянии на здоровье всех негативных факторов и возможностях уменьшения этих влияний; • повышается роль медицинских структур Компании в формировании здорового образа жизни работников, развивается профилактическая медицина; • совершенствуется работа подведомственных спортивно-оздоровительных учреждений; • обеспечиваются массовые занятия оздоровительными тренировками. |
 | ОАО "Дальневосточная распределительная сетевая компания" С целью профилактики заболеваний и пропаганды здорового образа жизни в Компании развивается корпоративный спорт. Сотрудники принимают участие в городских, региональных, областных соревнованиях. В ОАО "ДРСК" проводится "Антитабачная политика": — полный запрет курения на рабочих местах; — осуществление стратегий, помогающих курящим отказаться от курения (методы и подходы, поддерживающие и стимулирующие людей в их желании отказаться от курения); — разъяснения о вреде курения, о пагубных последствиях как для самих курящих, так и для окружающих работников "при пассивном" курении. Использование публикаций в СМИ, вывешивания статей и материалов на стендах по охране труда и пр. |
 | ПАО "Северсталь" реализуется комплексная программа "Здоровье Северстали", включающая в т.ч. такие направления, как: — Обеспечение полноценным питанием. Объединение "цехов питания" (40 предприятий питания, расположенных прямо в промышленной зоне). Их главная задача — обеспечить высокое качество приготовления пищи и ее сбалансированность на основе внедрения современных технологических линий, с максимально удобным для металлургов сервисом, приближенным к рабочему месту. — Физкультурно-оздоровительные программы. К услугам металлургов предоставляется современно оснащенная спортивная база: стадион "Металлург", физкультурно-оздоровительный комплекс, ледовый комплекс "Алмаз", "ДОМ Физкультуры" с плавательным бассейном и залами для занятий фитнесом, Дворец Спорта, стрелковый тир, спортивный комплекс "Юбилейный", лыжная база с загородным стадионом. |
 | АО "СУЭК" Значительное место в реализации социальных программ СУЭК занимает сохранение и укрепление здоровья сотрудников, продление активного трудового долголетия. Компания уделяет особое внимание развитию спорта и популяризации здорового образа жизни среди своих сотрудников и населения регионов присутствия. С 2011 г. в компании реализуется программа "Здоровье", важной и неотъемлемой ее частью является спорт. Цель программы: создание условий для сохранения и укрепления здоровья работников. Задачи программы: — пропаганда здорового образа жизни; — создание условий для занятий физической культурой и спортом, направленных на укрепление здоровья и организацию активного отдыха граждан всех возрастных категорий; — формирование потребности в здоровом образе жизни. Кроме того, в компании реализуется "Профилактическая программа по борьбе с курением". Цель программы: улучшение и сохранение здоровья работников и продление активного долголетия путем антитабачной пропаганды, оказания медицинской помощи и проведения мероприятий, направленных на профилактику и отказ от курения. Задачи программы: — соблюдение прав работников компании в сфере охраны здоровья от воздействия окружающего табачного дыма и последствий потребления табака; — предупреждение заболеваемости, инвалидности, преждевременной смертности работников, связанных с воздействием окружающего табачного дыма и потреблением табака; — ответственность компании за обеспечение прав работников в сфере охраны здоровья от воздействия окружающего табачного дыма и последствий потребления табака; — системный подход при реализации мероприятий, направленных на профилактику табакокурения, сокращение потребления табака, непрерывность и последовательность их реализации; — взаимодействие с медицинскими и общественными организациями в реализации профилактических программ и пропаганды отказа от курения; — информирование работников компании о вреде потребления табака и вредном воздействии окружающего табачного дыма. |
 | ПАО "Фосагро" Реализуется программа "Поддержка здоровья и здорового образа жизни". Направления программы: — профилактика и укрепление здоровья сотрудников; — профилактика профессиональных заболеваний; — обеспечение условий для полноценного восстановления и повышения работоспособности; — организация оздоровительного отдыха сотрудников; — организация физкультурно-спортивных и оздоровительных мероприятий. Особое внимание уделяется организации питания работников. Осуществляется ежеквартальная оценка качества питания. Для работников с вредными условиями труда организована выдача лечебно-профилактического питания, молока. Ежемесячно во всех столовых организуются тематические дни. С 2014 г. ежегодно проводятся конкурсы профессионального мастерства с целью повышения уровня профессиональной подготовки и привлечения молодежи в команду ООО "Корпоративное питание". Работники компании имеют возможность ежедневно пользоваться услугами современных спортивных комплексов, расположенных непосредственно рядом с рабочими местами. |
 | ОАО "РЖД" В компании активно реализуются программы здоровой среды и здорового образа жизни, включающие в т.ч. такие направления, как: — первичная профилактика заболеваний работников локомотивных бригад; — очищение организма и снижение веса; — "АНТИСТРЕСС"; — "АНТИТАБАК"; — "АКТИВНЫЙ ОТДЫХ". В НУЗ ОАО "РЖД" разрабатываются памятки и рекламный материал с комплексом производственной гимнастики на рабочем месте, формируются группы здоровья для проведения занятий ЛФК, других оздоровительных занятий, в трудовых коллективах проводятся просветительские мероприятия в целях информирования работников о необходимости обращения в медицинские учреждения в профилактических целях, уделяется внимание поддержанию здорового образа жизни. |
 | ФГБУ "НМИЦ ТПМ" Минздрава России Разработан и реализуется большей частью сотрудников организации авторский комплекс физических упражнений для разного уровня подготовки, в т.ч. гимнастика для офисных работников, позволяющая снять напряжение и укрепить различные группы мышц. |
Отдельные практики и мероприятия, представленные работодателями в рамках исследования ФГБУ "НМИЦ ТПМ" Минздрава России "Лучшие практики корпоративных программ"
Московская область. Муниципальное бюджетное учреждение "Конькобежный центр "Коломна"
(278 человек)
Проводятся регулярные спортивные игры как отличный способ увлекательно и с пользой провести свободное время после работы, способствующие развитию командного духа в коллективе, укреплению отношений между сотрудниками. Спартакиада трудового коллектива и День физкультурника проводятся с целью укрепления здоровья и привлечения активного населения к систематическим занятиям физической культурой и спортом.
Результаты мероприятий. Доля работников, снизивших массу тела, составила 10%.

Челябинская область, г. Миасс, АО "Автомобильный завод "УРАЛ" (8000 человек)
Проводится фитнес-марафон "Худеем вместе за 55 дней!", главная цель которого мотивировать работников предприятия к ведению здорового образа жизни и сформировать у участников фитнес-марафона здоровые привычки (рациональное питание и достаточная физическая активность).


Ростовская область, поселок Зимовники, Муниципальное учреждение культуры "Межпоселенческая центральная библиотека" Зимовниковского района (54 человека)
Мероприятие "Брось курить и победи". В ходе мероприятия рассуждали о причинах появления вредных привычек — слабость характера. Узнали, какие три правила нужно выполнять, чтобы не стать рабом вредных привычек: не скучать, найти себе занятие по душе; узнавать мир и интересных людей. Рассказывали, какой вред курение наносит здоровью человека и призывали курильщиков хотя бы на один день воздержаться от пагубной привычки, а тех, кто не курит, — никогда не брать в руки сигарету.

Оренбургская область, филиал "Оренбургский" Публичного акционерного общества "Т Плюс"
(2117 человек)
Комплексная программа по улучшению здоровья сотрудников, формированию принципов рационального питания и мотивации к здоровому образу жизни.
Мероприятия программы:
- Анкетирование сотрудников для оценки распространенности факторов риска.
- Проведение комплексного обследования на выявление факторов риска в мобильном центре здоровья ГБУЗ "ООЦОЗМП".
- Анализ показателей здоровья работников предприятия и оценка результатов обследования на факторы риска НИЗ.
- Внедрение мероприятий меняющих поведение работников:
4.1. Участие в проекте "Стройный режим" совместно с ГБУЗ "ООЦОЗМП" (онлайн-интенсив курс по снижению веса и оздоровлению организма с диетологом-нутрициологом).
4.2. Распространение информационного материала о правильном питании в доступных местах на стендах (листовки, буклеты, плакаты).
4.3. Проведение информационно-мотивационных кампаний на территории предприятия (рассылка тематического контента по всем существующим каналам связи).
4.4. Обеспечение работников чистой питьевой водой (обеспечение доступа к питьевой воде).
4.5. Поддержание мест для приема пищи работников, оборудованных раковиной с водой, столом, стульями, посудой, чайником, холодильником и техникой для разогрева пищи.
4.6. Проведение выездной лекции "Рациональное питание" совместно с ГБУЗ "ООЦОЗМП".
4.7. Проведение корпоративных конкурсов: "Рецепты для здоровья", "Полезный завтрак".
4.8. Проведение выездного приема врача диетолога совместно с ГБУЗ "ООЦОЗМП".
- Мониторинг и оценка эффективности внедрения мероприятий, коррекция мероприятий с учетом достигнутых результатов.


По подпрограмме "Забота о семье"
Опыт Вологодской области
В МУП "Коммунальные системы" г. Сокол предусмотрены:
трудоустройство несовершеннолетних детей работников предприятия;
оказание за счет средств предприятия материальной помощи при рождении ребенка;
оплата до 70% от полной стоимости путевок в детские оздоровительные лагеря и санатории для детей работников предприятия;
организация новогодней елки и подарков за счет средств предприятия и других финансовых источников для детей;
предоставление работнику дополнительных оплачиваемых дней с сохранением среднего заработка (в случаях рождения ребенка отцу при выписке жены из роддома; 1 сентября матери (отцу) первоклассника; предоставление материальной помощи на подготовку к школе первоклассника.
Также на предприятии организуются конкурсы творческих работ среди детей с целью активизации творческого потенциала семей работников и вовлечения семей в корпоративную жизнь предприятия. По итогам конкурса победители и призеры награждаются дипломами и подарками.
На АО "Оптико-механический завод" проходит психологическое консультирование по вопросам материнства и отцовства, занятия по подготовке к беременности и родам, предоставляется гибкий график работы, пособие от работодателя за рождение ребенка, выплата материальной помощи, работает психолог на постоянной основе.
АО "Череповецкий фанерно-мебельный комбинат" с сентября 2023 г. запустило ряд спортивных проектов психологического стимулирования:
- "Фитнес с мамой". На предприятии созданы условия для занятий фитнессом сотрудников, которые находятся в декретном отпуске. Молодые мамы приходят два раза в неделю вместе с малышом, занимаются силовыми тренировками, ВИИТ (высокоинтенсивный интервальный тренинг) или танцевальной аэробикой.
- "Маугли" —общая физическая подготовка для детей работников комбината в возрасте от 3-7 лет.
- "Своя ноша не тянет" —чемпионат (веселые старты) по переноске жен на приз генерального директора.
АУ СО ВО "Дом социального обслуживания "Сосновая Роща" проводят для сотрудников и членов их семей тимбилдинг "Мудрость цивилизаций", спортивные занятия зумба, фитнес-занятия, степ-аэробику, скандинавскую ходьбу, игровые программы "Скакалочные состязания", "Спортивная солянка", "Основы здорового питания" и т.д., командные спортивные мероприятия "Полоса препятствий", "25000 шагов к здоровью".
Опыт Луганской Народной Республики
- В ГБУЗ "Луганская городская поликлиника" на мультимедийном экране в поликлинике демонстрируются видеоматериалы, посвященные тематике репродуктивного здоровья по определенным дням недели. В Международный день беременных в женской консультации всем беременным, состоящим на учете, проводится торжественное занятие — школы беременных, чествование будущих мам и вручение каждой женщине символических подарков за счет медицинской организации, это событие отражается на медиаэкране поликлиники и в СМИ.
- БУЗ "Луганская городская поликлиника № 12" по внутриполиклиническому радио проводятся беседы на темы сохранения репродуктивного здоровья.
- ГБУЗ "ЛГКМБ № 1": в гинекологическом отделении проводится торжественное чествование беременных, находящихся на стационарном лечении в Международный день беременных, проведение круглого стола с вручением подарков будущим мамам.
- Луганским республиканским центром здоровья разработаны многочисленные буклеты и памятки для распространения в организованных коллективах по разным темам репродуктивного здоровья, полового воспитания, образования будущих отцов и матерей.
Комплексная программа, включающая несколько направлений, обеспечивающих сохранение и укрепление репродуктивного здоровья
Опыт Смоленской области
Программа "Здоровый сотрудник" для работающего населения города Смоленска и Смоленской области как типовая модельная программа.
Основными задачами корпоративной программы по укреплению здоровья сотрудников являются:
- Формирование системы мотивации работников организации к здоровому образу жизни, включая здоровое питание и отказ от вредных привычек.
- Содействие прохождению работниками профилактических осмотров и диспансеризации.
- Создание благоприятной рабочей среды (сплочение коллектива) для укрепления ментального здоровья и благополучия организации.
- Повышение ответственности за индивидуальное здоровье и приверженности к здоровому образу жизни работников и членов их семей.
- Сохранение на длительное время здоровых трудовых ресурсов.
- Повышение производительности труда.
- Сокращение трудопотерь по болезни, из-за презентеизма и абсентеизма.
Достижение цели обеспечивается за счет проведения для работников профилактических информационно-образовательных мероприятий по основным направлениям модельных практик:
- "Профилактика потребления табака";
- "Снижение потребления алкоголя с вредными последствиями";
- "Здоровое питание и рабочее место";
- "Повышение физической активности";
- "Сохранение психологического здоровья и благополучия";
- "Сохранение женского и мужского здоровья";
- "Сохранение стоматологического здоровья".
На входе было проведено анкетирование всех участников корпоративной программы. Результаты анкетирования показали следующее:
- Опрошенные сотрудники в целом ответственно относятся к своему здоровью, регулярно проходят диспансеризацию и (или) профилактический медосмотр (хотя есть путаница в понимании между прохождением диспансеризации определенных групп населения/профилактического медицинского осмотра и периодическим медицинским осмотром в рамках мероприятий по охране труда).
- Сотрудники, как правило, знают свои цифры артериального давления.
- Барьерами к использованию возможностей для ведения здорового образа жизни на рабочем месте, по мнению респондентов, являются отсутствие спортивных объектов на работе, отсутствие профилактория и финансовой поддержки мероприятий по оздоровлению.
- Поведенческие факторы риска ХНИЗ присутствуют практически у всех сотрудников в количестве 2-3 и более факторов риска у каждого сотрудника.
- Сотрудники с интересом относятся ко всем разделам, большой запрос по вопросам "Сохранение женского и мужского здоровья" и "Сохранение психологического здоровья и благополучия".
На основании полученных результатов опроса была сформирована результат-ориентированная программа сохранения здоровья и формирования здорового образа жизни для каждого коллектива сотрудников.
Информационно-образовательный блок для сотрудников
— частота проведения — 1-4 раза в мес.;
— продолжительность — 30-45 мин;
— информационно-методические наглядные материалы предоставляются в долгосрочное пользование по каждой теме в электронном виде.
Тематика:
- Check-up "Женское здоровье". Что должна делать женщина, чтобы быть здоровой.
- Check-up "Мужское здоровье". Что должен делать мужчина, чтобы быть здоровым.
- Бережное отношение к себе и окружающим. Психологическая забота и эмпатия — залог ментального здоровья и экологичного общения.
- Индивидуальная профилактика ХНИЗ: новеллы о факторах риска.
- Физическая активность: встань со своего стула и иди!
- Функциональное питание: белки, жиры и углеводы, микроэлементы, клетчатка и витамины. Чего и сколько в граммах?
- Метеочувствительность, метеозависимость и здоровье.
- Оказание первой помощи при неотложных состояниях.
- Профилактика остеопороза.
- Твое здоровье в твоих руках: мастер-класс по профилактике рака груди.
- Витальность как основа и ресурс для опоры и поддержки.
Предоставлена презентация по оказанию неотложной помощи в критических состояниях (гипертонический криз, приступ стенокардии, острое нарушение мозгового кровообращения, сердечная недостаточность, внезапная смерть).
Переданы видеоролики с комплексами производственной гимнастики для офисных сотрудников (преимущественно сидячая работа) и для работающих людей зрелого возраста.
Предоставлены в долгосрочное пользование пакеты информационных материалов в электронном презентационном виде:
- 1. Профилактика артериальной гипертонии.
- Рациональное питание.
- Профилактика избыточного веса.
- Физическая активность.
- Профилактика табакокурения.
- Профилактика стресса.
- Если Вы мужчина…Если Вы женщина…
Опыт Воронежской области
В Воронежской области организовано поведение информационно-просветительских мероприятий, направленных на улучшение репродуктивного здоровья молодежи. 16 апреля и 14 мая 2024 г. на базе Воронежского государственного медицинского университета им. Н. Н. Бурденко и Воронежского государственного университета состоялись мероприятия из цикла "Здоровое отношение к себе — основа репродуктивного здоровья".
Целью данного мероприятия являлось развитие у молодежи нравственных основ для построения здорового отношения к себе, здоровых отношений с другими людьми, здоровой семьи через адаптированную к студенческой среде интерактивную форму психологического тренинга.
В качестве организаторов встречи выступили Министерство здравоохранения Воронежской области, ВГМУ им. Н. Н. Бурденко, ВФ АО СК "СОГАЗ-Мед" и группа компаний "ОЛИМП здоровья".
Для ведения диалога с участниками приглашаются самые известные и квалифицированные психотерапевты и психологи города:
- Заведующая кафедрой психологии и поведенческой медицины ВГМУ им. Н. Н. Бурденко, к.м.н. Е. А. Кудашова
- Врач-психотерапевт, семейный психолог, нейрокоуч группы компаний "Олимп здоровья" Н. М. Шестакова
- Главный внештатный психолог Министерства здравоохранения Воронежской области по планированию семьи А. А. Карпенко.
В рамках мероприятий проводится авторский тренинг "Здоровое отношение к себе — основа репродуктивного здоровья" с интерактивной обратной связью от участников, которые в течение тренинга активно взаимодействуют с психологом, отвечая анонимно в режиме онлайн на вопросы в своих смартфонах. Ответы выводятся на экран и анализируются. Тренинг построен на коротких вводных эпизодах-эссе об основных аспектах проявления личности во взаимоотношениях с окружающими, критериях определяющих "здоровье" отношений, их ценность и нравственность. После каждого эпизода идет короткая обратная связь с участниками, позволяющая оценить себя в предлагаемой ситуации, задуматься о своем поведении и его возможной коррекции.
В рамках мероприятия нейрокоуч и практик-консультант также проводят мастер-класс "Как сохранить психологическое здоровье в токсичных отношениях" на практических упражнениях для поддержания своего психологического здоровья, а также рассматривают возможные негативные последствия таких отношений, включая потери для здоровья.
Главный внештатный психолог задает вопросы аудитории по поводу желаемого количества детей, показывает муляжи человеческих зародышей разного срока беременности, выполненных в натуральную величину из специального тактильного материала, рассказывает, что и на каком этапе развития плода происходит.
Также в рамках данного мероприятия акцентируется внимание на необходимость регулярных обследований в области репродуктивного здоровья, информирование студентов о возможности проверить свое репродуктивное здоровье в рамках диспансеризации по полису ОМС.
Кроме того, вниманию участников мероприятия представляются возможности телеграмм-бота "Навигатор здоровья", цель которого — выявление проблем, связанных с репродуктивным здоровьем. Так, все участники проходят анонимное анкетирование по состоянию репродуктивного здоровья. При наличии ответов, представляющих риски здоровью, программа предлагает записаться на бесплатную консультацию врача-уролога или врача-гинеколога в группу компаний "Олимп здоровья" или переключает на запись к врачам государственных поликлиник города.
В завершение мероприятия страховые представители Воронежского филиала АО "СК "СОГАЗ-Мед" разыгрывают спонсорские призы для присутствующих студентов. При входе каждый участник получает номерок, который крутится в барабане и имеет шанс выиграть билет в популярные молодежные заведения или сертификат на услуги в частной клинике.
В общей сложности мероприятие посетило более 400 студентов различных курсов и факультетов ВГМУ им. Н. Н. Бурденко и ВГУ, студентами отмечена высокая актуальность данной темы, эффективный формат преподнесения информации и ценность практических советов.
Данная работа в регионе продолжается, запланированы информационно-просветительские мероприятия в другие крупные ВУЗы.

Приложение 4
МЕЖДУНАРОДНЫЕ ПРАКТИКИ РЕАЛИЗАЦИИ КОМПЛЕКСНЫХ КОРПОРАТИВНЫХ ПРОГРАММ СОХРАНЕНИЯ И УКРЕПЛЕНИЯ РЕПРОДУКТИВНОГО ЗДОРОВЬЯ 5
Компании финансового сектора
Monzo Bank известен своей корпоративной культурой и приверженностью к сохранению репродуктивного здоровья своих сотрудников. Все сотрудники данной организации имеют доступ к собственной клинической команде для проведения неограниченных экспертных консультаций. Клиническая команда помогает сотрудникам Monzo Bank пройти через менопаузу, улучшить показатели репродуктивного здоровья, планировать создание семьи. Клиническая команда также предоставляет сотрудникам Monzo Bank доступ к набору образовательных ресурсов, охватывающих некоторые из наиболее сложных и распространенных проблем репродуктивного здоровья.
Bain Capital и Rathbones поддерживает своих сотрудников в лечении бесплодия, предлагая страхование программ экстракорпорального оплодотворения (ЭКО). Это означает, что сотрудники имеют доступ к неограниченным и полностью компенсируемым циклам ЭКО, которыми они смогут воспользоваться, когда захотят создать или расширить свою семью. Помимо программы ЭКО, в перечень оплачиваемых услуг входят: замораживание яйцеклеток, поддержка и лечение в период менопаузы (включая назначения заместительной гормональной терапии), раннее выявление и лечение мужских онкологических заболеваний (рак предстательной железы и рак яичек), а также синдрома поликистозных яичников и эндометриоза, поддержка программ суррогатного материнства и усыновления.
American Express обеспечивает полную компенсацию расходов на суррогатное материнство, усыновление или лечение бесплодия в размере до 35 000 долларов США, а также бесплатную доставку грудного молока для любого сотрудника, путешествующего по делам компании.
Rothesay предоставляет своим сотрудникам доступ к неограниченным клиническим консультациям врачами-специалистами и поддержке на протяжении всего периода их фертильности, формирования семьи и менопаузы. Политика поддержки рождаемости Rothesay гарантирует, что некоторые виды лечения бесплодия будут частично возмещены. Дополнительный оплачиваемый отпуск также предоставляется работникам, если они или их партнер проходят лечение от бесплодия.
Компании розничной торговли
Lululemon предоставляет своим сотрудникам доступ к неограниченным клиническим консультациям врачами-специалистами по вопросам менопаузы, женского и мужского здоровья.
Amazon оказывает комплексную финансовую поддержку репродуктивного здоровья всем своим сотрудникам, в т.ч. при предоставлении услуг по замораживанию яйцеклеток и ЭКО.
ASDA разрешает своим сотрудникам до трех периодов оплачиваемого отпуска для проведения ЭКО: пять дней для женщин и один день для мужчин, а также возможность менять смены в соответствии с назначениями и дополнительный неоплачиваемый отпуск при необходимости.
Компании, оказывающие юридические услуги
Osborne Clarke предоставляет своим сотрудникам доступ к специалистам в области репродуктивного здоровья для решения всех проблем, связанных с менопаузой, фертильностью, формированием семьи, мужским и женским здоровьем. Репродуктивное здоровье женщин включает руководство и поддержку в период менопаузы, лечения заболеваний, передающихся половым путем, миомы матки, эндометриоза, синдрома поликистозных яичников и других состояний. Репродуктивное здоровье мужчин включает проведение раннего скрининга на выявление рака предстательной железы и яичек, а также сексуального здоровья.
Foot Anstey предоставляет сотрудникам доступ к экспертным ресурсам по вопросам фертильности, менопаузы и любым другим проблемам, связанным с репродуктивным здоровьем. Компания также предлагает сотрудникам финансовую компенсацию за стационарное лечение в размере до 15 000 фунтов стерлингов.
Slaughter and May предоставляет пособия на лечение репродуктивного здоровья и формирования семьи, а также финансовые взносы на услуги по замораживанию яйцеклеток. Кроме того, в компании предусмотрена повышенная оплата отпуска по семейным обстоятельствам и совместный отпуск по уходу за ребенком.
Cooley предлагает возмещение до 450 00 фунтов стерлингов за лечение бесплодия среди своих сотрудников.
Компании технологического сектора
Meta 6 предлагает комплексные льготы по репродуктивному здоровью всем своим сотрудникам. За лояльность компании сотрудникам Meta предлагается широкий спектр услуг в области репродуктивного здоровья посредством поддержки программ фертильности и формирования семьи, помощь женщинам в менопаузе, иные программы укрепления мужского и женского здоровья.
Spotify делает охрану репродуктивного здоровья доступной для всех своих сотрудников. В Spotify выплачивается пособие за рождение ребенка и оплачивается отпуск по беременности и родам или отцовству.
Microsoft недавно взяла на себя обязательство предложить своим сотрудникам комплексную поддержку репродуктивного здоровья посредством услуг по лечению бесплодия и менопаузы. Сюда входят расходы, связанные с ЭКО, до 15 000 долларов США, включая лекарства и процедуры. Данная льгота доступна всем сотрудникам, проработавшим в компании не менее одного года. Кроме того, Microsoft предлагает покрытие до двух циклов замораживания яйцеклеток для женщин.
Компании из отрасли энергетики и промышленности
ICMM дает возможность своим сотрудникам получать поддержку со стороны собственной клинической команды посредством экспертного и конфиденциального лечения и консультаций по всем проблемам репродуктивного здоровья. Это включает в себя лечение бесплодия, замораживание яйцеклеток, проведение ЭКО и поддержку программ суррогатного материнства, медицинского обслуживания при симптомах менопаузы и перименопаузы, включая рекомендации по образу жизни и выписку рецептов для проведения заместительной гормональной терапии (при необходимости), решение проблем со здоровьем мужчин и женщин, таких как синдром поликистозных яичников, миома матки и эндометриоз.
BP предлагает до 15 000 фунтов стерлингов на лечение бесплодия для женщин и их партнеров, а также поддержку в виде подкастов, поддержки коллег, вебинаров и круглых столов. Менеджеры также получают рекомендации по вопросам рождаемости на рабочем месте, чтобы помочь поддержать свою команду. Вернувшимся из отпуска предлагается карьерный коучинг, а линейным менеджерам предоставляются контрольные списки и обучение тому, как успешно соблюдать баланс времени между работой и семейной жизнью. Женщины в период менопаузы могут получить доступ к группе поддержки и персональному плану медицинского обслуживания.
Американская компания Tesla, производящая электромобили, предлагает своим сотрудникам льготы: все сотрудники могут получить доступ к услугам по лечению бесплодия, включая ЭКО, а также услуги по заморозке яйцеклеток или спермы, получив при этом финансовую помощь от компании. Tesla также предлагает поддержку в покрытии судебных издержек, связанных с усыновлением и суррогатным материнством, что делает ее инклюзивной компанией, предлагающей ряд вариантов создания семьи.
II. ИНЫЕ ПРОГРАММЫ 7
Интегральная программа HUSKY INJECTION MOLDING SYSTEMS LTD 8 (Производство станков, Канада).
Компания Husky стремится активно интегрировать свои ценности здоровья и безопасности на всех уровнях рабочего места. У Husky есть оснащенный оздоровительный центр, который полностью субсидируется, и сотрудникам предлагается доступ к его услугам. Центр предлагает различные виды поддержки, которые могут быть полезны для беременных сотрудниц, включая врача-натуропата, массажиста, мануального терапевта и физиотерапевтов. Стоимость любых добавок, которые предназначены для беременных, например, фолиевой кислоты, покрывается до 75%.
Оздоровительная программа LINDA LUNDSTROM INC. (Дизайн и производство одежды, Канада). Компания придерживается политики и практики, которые поддерживают беременных работниц. По своей сути это всесторонняя оздоровительная программа, которая включает в себя 5 оплачиваемых оздоровительных дней. Женщинам предоставляется дополнительное время для посещения врача и для приспособления к возможной утренней тошноте. Для отдыха предусмотрены удобные зоны отдыха. Цеховой врач может помочь работникам при проблемах с репродуктивным здоровьем
CHATHAM KENT HEALTH UNIT. (Ассоциация учреждений здравоохранения, Канада). Первоначально отдел здравоохранения г. Чатем в графстве Кент провел обследование 500 рабочих мест для оценки общих потребностей, связанных со здоровьем. Опрос включал раздел о репродуктивном здоровье на рабочем месте. Результаты опроса показали, что необходимо сосредоточиться на создании рабочих мест, благоприятных для беременных. В ответ медицинское подразделение разослало информационные пакеты и продемонстрировало плакаты на различных рабочих местах. Они также организовали семинары по вопросам беременности и работы для работодателей, в том числе представителей здравоохранения и безопасности, сотрудников отдела кадров и медицинских сестер по гигиене труда. Тех, кто обладает специальными знаниями в этой области, пригласили выступить на семинарах.
Мероприятия для работодателей NIAGARA HEALTH UNIT. (Ассоциация учреждений, Канада). Инициатива "Оздоровление на рабочем месте в Ниагаре" была создана в 1999 г. и контролируется представителями всех подразделений Отдела здравоохранения. Инициатива Workplace Wellness в Ниагаре включает ежегодный симпозиум для работодателей в Ниагарском регионе. Он достигает большого количества рабочих мест и лиц, занимающихся охраной труда и безопасностью на рабочем месте. Другие виды деятельности Workplace Wellness в Ниагаре включают разработку информационных материалов по беременности и труду, предназначенных для различной аудитории, включая беременных женщин и их семьи, работодателей и общество в целом. Ярмарки здоровья были организованы на различных рабочих местах.
III. ОТДЕЛЬНЫЕ МЕРОПРИЯТИЯ, КОТОРЫЕ МОГУТ БЫТЬ ОТНЕСЕНЫ К СООТВЕТСТВУЮЩИМИ ПОДПРОГРАММАМИ
К подпрограмме "Ранняя диагностика и своевременное лечение заболеваний мочеполовой системы"
В качестве примера реализации комплексного подхода к информированию работодателей об актуальности заболеваний мочеполовой системы может быть рекомендована кампания по повышению осведомленности об урологических заболеваниях "Месяц осведомленности об урологии"9. В качестве мер, направленных на повышение осведомленности и поддержки сотрудников, предлагается:
— учитывать необходимость рационального размещения туалетных комнат на рабочем месте;
— обеспечивать возможность для регулярного питья воды (пить больше воды полезно для мочевого пузыря, снижается уровень концентрации мочи, а следовательно, и раздражающее воздействие на стенки мочевого пузыря);
— информировать работодателей о необходимости мотивировать и помогать сотрудникам организации в осознании необходимости поддержания здорового веса, ограничения потребления алкоголя и кофеина, а также поддержания физической формы и выполнения комплекса упражнений для укрепления тазового дна;
— поощрение использования оздоровительных услуг, возможно, проведение занятий по медитации. Исследования показывают, что медитация может помочь при эпизодах гиперактивного мочевого пузыря;
— поощрять регулярные осмотры и проведение скрининговых исследований для выявление урологических проблем;
— проводить широкое обсуждение на рабочем месте вопросов здоровья как женщин, так и мужчин, не считая данные темы табуированными.
К подпрограмме "Оценка репродуктивного здоровья для создания семьи"
В качестве эффективного инструментария для выявления факторов риска нарушения репродуктивного здоровья рекомендуется также использовать комплекс опросников, анкет, выявляющих социальные детерминанты здоровья с последующей стратификацией риска.
Примерами таких анкет могут являться опросники Шкала старения мужчин (Ageing male scale), Международный индекс эректильной функции (International index of erectile function), Японская шкала риска метаболического синдрома (Japanese Metabolic Syndrome Risk Score), Протокол для реагирования и оценки активов, рисков и опыта пациентов (Protocol for responding to and assessing patients’ assets, risks, and experiences).
Степень риска для репродуктивного здоровья может быть разделена на 3 группы.
— "зеленая" — к которой относятся работники, не имеющие выраженных факторов риска репродуктивных нарушений и не требующие консультаций врачей-специалистов;
— "желтая" — к которой относятся работники, имеющие поведенческие и иные факторы риска репродуктивных нарушений, которые могут в ближайшие 5 лет привести к заболеваниям репродуктивной системы. Данные работники нуждаются в плановой консультации;
— "красная" — к которой относятся работники, уже имеющие заболевания репродуктивной системы или факторы риска, которые могут непосредственно привести к заболеваниям репродуктивной системы. Данная категория работников требует направления для консультации к специалисту по репродуктивному здоровью.
Организация этой работы требует создание консультативного кабинета и подготовки специалистов. Консультировать сотрудников могут врач, средний медицинский работник или медицинский психолог. Если в организации уже существует кабинет профилактической помощи, необходимо дополнить его функции оказанием консультативной помощью сотрудникам с риском репродуктивных нарушений.
Информация о пациентах, результатах их обследования в соответствии с назначенными группами риска передается в региональный Центр общественного здоровья и медицинской профилактики для внесения в репродуктивный регистр для формирования дальнейшей персонализированной программы реабилитации.
К подпрограмме "Репродуктивное здоровье без факторов риска хронических неинфекционных заболеваний"
Для увеличения приверженности мужчин к участию в мероприятиях медицинского характера, позволяющих выявить факторы риска развития ХНИЗ, может быть использован простой и наглядный подход, ориентированный на принцип проведения аналогий между человеческим организмом и внешними системами. В качестве примера может быть рекомендована программа Pit Stop 10. Это оздоровительная программа, целью которой является привлечение мужчин всех возрастов путем сопоставления частей тела с частями автомобиля. Она выполняется в виде серии станций, каждая из которых включает в себя быструю и простую проверку состояния здоровья. Оформление станций "Пит стоп" организуется в немедицинской манере, и это позволяет участникам преодолеть любые опасения, которые у них могут возникнуть по поводу обращения к врачу.
Особенности программы формируются в мужской, механистической концепции, которая включена в серию мужских скрининговых тестов и обеспечивает вовлекающий комфортный фон с элементами юмора.
Программа использует "автомобильную" тему, чтобы донести свое сообщение. Например, есть "станции", которые предполагают неинвазивное медицинское обследование; "Механики здоровья" обсуждают "проверку ходовой части" (окружность живота), "свечи зажигания" (репродуктивное здоровье), "давление масла" (кровяное давление), "присадки к топливу" (потребление алкоголя), "амортизаторы" (навыки преодоления трудностей). После того, как участники пройдут через "Пит стоп", они получат наклейку "пригодные к эксплуатации" или "непригодные". Тем, кто получает последний, рекомендуется проконсультироваться с врачом-терапевтом или врачом общей в практики (семейным врачом).
Мероприятие можно проводить там, где находятся мужчины, в том числе: сельскохозяйственные предприятия, торговые центры, фестивали и т.д.
Еще одной практикой может являться Программа укрепления здоровья на рабочем месте "POWERPLAY" 11, целью которой является поощрение постепенного увеличения физической активности и приверженности здоровому питанию с использованием соревновательного компонента. Для поддержки этих направлений рабочие места рекомендуется снабдить печатными материалами и ресурсами по внедрению мероприятий, (например, еженедельные советы по цифровым инструментам, плакаты для отслеживания прогресса, журналы команд). Программу необходимо реализовывать в течение 6-месячного периода в формате дружеской конкуренции между сотрудниками, а также между рабочими местами с применением цифровых инструментов (например, шагомеры, фитнес-трекеры) для улучшения самоконтроля физической активности и здорового пищевого поведения. В структуре адаптированной к российским условиям программы рекомендуется предусмотреть следующие пять шагов:
- "Шаг вверх". Мужчины бросают друг другу вызов и соревнуются как команда, чтобы набрать наибольшее количество шагов во время виртуального путешествия по длительному маршруту (например, в Российской Федерации — по Золотому кольцу). У каждой команды есть 4 недели, чтобы накопить шаги, пока они "путешествуют" по избранному маршруту. Команда, преодолевшая наибольшую дистанцию в конце 4-х недель, становится победителем. Мужчины будут отслеживать свои шаги на смартфоне или при помощи фитнес-трекера.
- "Заправься". Мужчины должны соревноваться, как хоккейная команда и набрать наибольшее количество голов, выполнив действия, указанные в специальных карточках. Каждая карточка имеет квадраты, которые обозначают задачи для выполнения, связанные со здоровым питанием и физической активностью (например, ели здоровую закуску вместо фаст-фуда), а также 3 квадрата "по собственному выбору". В итоге мужчинам рекомендуется продолжать быть физически активными при выборе здоровой пищи.
- "Будь начеку". Мужчины в индивидуальном порядке бросают друг дугу вызов, в том, чтобы, участвуя в случайных актах доброты, помочь своим коллегам и продвигать позитивную культуру на рабочем месте посредством командной работы и товарищества. Сотрудники признают добрые поступки, перемещая бумажные шайбы в сторону ворот по большому плакату, изображающему хоккейное поле. Тренер на рабочем месте может подсчитывать еженедельные итоги на электронном табло.
- "Плати по счетам". Мужчины каждую неделю проявляют здоровую активность, чтобы уменьшить зависимость от курения и бросить курить. Мужчины получают колоду из 52 карт действий. В карточках указаны задачи, которые необходимо выполнить. Данные задачи поддерживают мужчин независимо от того, где они находятся на пути избавления от курения (например, в Российской Федерации — "Я просмотрел все материалы по отказу от курения на сайте takzdorovo.ru: Мне больше всего понравился этот материал"). Мужчины заполняют и сдают карточки тренеру на рабочем месте в обмен на небольшие призы и участвуют в розыгрыше большего приза.
- "Меняйся к лучшему". Работодатели или подразделения должны предпринимать конструктивные шаги для создания здоровой рабочей среды. Формирование здоровой культуры, адаптированной к каждой уникальной среде, посредством изменений в окружающей среде и политике помогает сотрудникам вести здоровый образ жизни и приносит положительные выгоды для всей организации.
К подпрограмме "Забота о семье"
"ДЕНЬ ОТЦА" ("ДЕНЬ МУЖЧИНЫ")
Мероприятие направлено на повышение осознанности работников о факторах риска нарушений мужского здоровья, а также формирование традиционных семейных ценностей у работников-мужчин. "День отца" может включать несколько основных частей: оздоровительное тестирование (оценка риска возникновения ХНИЗ у мужчин, оценка психологических параметров взаимодействия в семье и др.), обучение (семинар по решению семейных проблем или психологических проблем, связанных с отцовством) и индивидуальные консультации (профилактическое, в т.ч. семейное консультирование).
"День отца" ("День мужчины") рекомендуется проводить на территории организации с использованием переговорных, актовых-залов или конференц-залов. Перед проведением мероприятия за 2-4 нед проводится коммуникационная кампания с целью вовлечения работников в программу. Ориентировочное количество участников в течение дня должно составлять 30-50 человек. Время отвлечения работника от профессиональных обязанностей составляет около 30 мин.
В процессе реализации мероприятия рекомендуется провести:
— оценку уровня психологических и иных навыков мужчин для жизни в семье;
— информирование работников о традиционных семейных ценностях, семейной психологии;
— обеспечение доступности консультаций и поддержка сформированных навыков ведения здорового образа жизни.
В рамках проведения "Дня мужчины" необходимо предусмотреть проведения семинаров и лекций для сотрудников на темы, связанные с мужским репродуктивным здоровьем: "Влияние вредных факторов производства на мужское репродуктивное здоровье", "Как сохранить мужское здоровье в современных условиях", "Стресс и здоровье мужчины", "Влияние поведенческих факторов риска (курение, употребление алкоголя) на мужское репродуктивное здоровье".
При проведении "Дня мужского здоровья" важно обращать внимание работников на то, по каким вопросам работники могут получать консультации, а также на то, что консультирование анонимное и соблюдается политика конфиденциальности.
Персонал, проводящий консультирования на рабочем месте, должен быть обучен методам мотивационного консультирования, когнитивно-поведенческой терапии и моделям изменения поведения.
1 Приказ Минздрава России от 28.01.2021 № 29н "Об утверждении Порядка проведения обязательных предварительных и периодических медицинских осмотров работников, предусмотренных частью четвертой статьи 213 Трудового кодекса Российской Федерации, перечня медицинских противопоказаний к осуществлению работ с вредными и (или) опасными производственными факторами, а также работам, при выполнении которых проводятся обязательные предварительные и периодические медицинские осмотры".
2 https://gnicpm.ru/wp-content/uploads/2020/01/korporativnye_modelnye_programmy_ukreplenie_obshhestvennogo_zdorovya.pdf
3 https://gnicpm.ru/public_health/korporativnye-programmy-ukrepleniya-zdorovya-rabotayushhih.html
4 Информация, полученная по результатам опроса работодателей в рамках исследования ФГБУ "НМИЦ ТПМ" Минздрава России "Лучшие практики корпоративных программ".
5 https://www.fertifa.com/post/companies-that-are-offering-reproductive-health-benefits.
6 Компания "Meta Platforms, Inc." признана экстремистской организацией и ее деятельность запрещена на территории Российской Федерации.
7 https://www.beststart.org/resources/wrkplc_health/pdf/WorkplaceDocum.pdf
8
9 https://cordellhealth.co.uk/urology-awareness-month-supporting-your-employees-and-breaking-taboos/
10 Программа реализуется в Австралии (штат Виктория).
11 Программа реализуется в Канаде (штат Британская Колумбия).
Список литературы
1. Gupta P, Gaines N, Sirls LT, Peters KM. A multidisciplinary approach to the evaluation and management of interstitial cystitis/bladder pain syndrome: an ideal model of care. Transl Androl Urol. 2015;4(6):611-19. doi:10.3978/j.issn.2223-4683.2015.10.10.
2. Management of Bladder Pain Syndrome: Green-top Guideline No. 70. BJOG. 2017;124(2):e46-e72. doi:10.1111/1471-0528.14310.
3. Rosenberg MT, Page S, Hazzard MA. Prevalence of interstitial cystitis in a primary care setting. Urology. 2007;69(4 Suppl):48-52. doi:10.1016/j.urology.2006.03.085.
4. Комяков Б.К., Очеленко В.А., Шевнин М.В. и др. Посткоитальный цистит как причина сексуальной дисфункции у женщин. Экспериментальная и клиническая урология. 2023;16(2):134-39. doi:10.29188/222285432023162134139.
5. Su CC, Sun BY, Jiann BP. Association of urinary incontinence and sexual function in women. Int J Urol. 2015;22(1):109-13. doi:10.1111/iju.12610.
6. Moradinasab S, Iravani M, Mousavi P, et al. Effect of cognitive-behavioral therapy on sexual self-esteem and sexual function of reproductive-aged women suffering from urinary incontinence. Int Urogynecol J. 2023;34(8):1753-63. doi:10.1007/s00192-023-05460-1.
7. Handa VL, Harvey L, Cundiff GW, et al. Sexual function among women with urinary incontinence and pelvic organ prolapse. Am J Obstet Gynecol. 2004;191(3):751-56. doi:10.1016/j.ajog.2003.11.017.
8. Nicolle LE. Asymptomatic bacteriuria: when to screen and when to treat. Infect Dis Clin North Am. 2003;17(2):367-94. doi:10.1016/s0891-5520(03)00008-4.
9. Barry R, Houlihan E, Knowles SJ, et al. Antenatal pyelonephritis: a three-year retrospective cohort study of two Irish maternity centres. Eur J Clin Microbiol Infect Dis. 2023;42(7):827-833. doi:10.1007/s10096-023-04609-6.
10. Habak PJ, Griggs Jr RP. Urinary Tract Infection in Pregnancy. In: StatPearls. Treasure Island (FL): StatPearls Publishing; July 4, 2023.
11. Dumanski SM, Eckersten D, Piccoli GB. Reproductive Health in Chronic Kidney Disease: The Implications of Sex and Gender. Semin Nephrol. 2022;42(2):142-52. doi:10.1016/j.semnephrol.2022.04.005.
12. Burgner A, Hladunewich MA. Women’s Reproductive Health for the Nephrologist. Am J Kidney Dis. 2019;74(5):675-81. doi:10.1053/j.ajkd.2019.04.017.
13. Ombelet W, Cooke I, Dyer S, Serour G, Devroey P. Infertility and the provision of infertility medical services in developing countries. Hum Reprod Update. 2008;14(6):605-21. doi:10.1093/humupd/dmn042.
14. Vander Borght M, Wyns C. Fertility and infertility: Definition and epidemiology. Clin Biochem. 2018;62:2-10. doi:10.1016/j.clinbiochem.2018.03.012
15. Boulicault M, Perret M, Galka J, et al. The future of sperm: a biovariability framework for understanding global sperm count trends. Hum Fertil (Camb). 2021;25(5):888-902.
16. Shanna H, Swan SC. How Our Modern World Is Threatening Sperm Counts, Altering Male and Female Reproductive Development, and Imperiling the Future of the Human Race. Scribner, New York 2020, 304 р.
17. Alshahrani S, McGill J, Agarwal A. Prostatitis and male infertility. J Reprod Immunol. 2013;100(1):30-6. doi:10.1016/j.jri.2013.05.004.
18. Alsaikhan B, Alrabeeah K, Delouya G, Zini A. Epidemiology of varicocele. Asian J Androl. 2016;18(2):179-81. doi:10.4103/1008-682X.17264.
19. Gorelick JI, Goldstein M. Loss of fertility in men with varicocele. Fertil Steril. 1993;59(3):613-16.
20. Wang H, Sun Y, Wang L, et al. Hypoxia-induced apoptosis in the bilateral testes of rats with left-sided varicocele: a new way to think about the varicocele. J Androl. 2010;31(3):299-305. doi:10.2164/jandrol.108.007153.
21. Boivin J, Bunting L, Collins JA, Nygren KG. International estimates of infertility prevalence and treatment-seeking: potential need and demand for infertility medical care [published correction appears in Hum Reprod. 2007;22(10):2800]. Hum Reprod. 2007;22(6):1506-12. doi:10.1093/humrep/dem046.
22. Eijkemans MJ, van Poppel F, Habbema DF, et al. Too old to have children? Lessons from natural fertility populations. Hum Reprod. 2014;29(6):1304-12. doi:10.1093/humrep/deu056.
23. Fanfair RN, Workowski KA. Clinical update in sexually transmitted diseases-2014. Cleve Clin J Med. 2014;81(2):91-101. doi:10.3949/ccjm.81a.13090.
24. Van Gerwen OT, Muzny CA, Marrazzo JM. Sexually transmitted infections and female reproductive health. Nat Microbiol. 2022;7(8):1116-26. doi:10.1038/s41564-022-01177-x.
25. Schuchardt L, Rupp J. Chlamydia trachomatis as the Cause of Infectious Infertility: Acute, Repetitive or Persistent Long-Term Infection? Curr Top Microbiol Immunol. 2018;412:159-82. doi:10.1007/82_2016_15.
26. Mårdh PA. Tubal factor infertility, with special regard to chlamydial salpingitis. Curr Opin Infect Dis. 2004;17(1):49-52. doi:10.1097/00001432-200402000-00010.
27. Leos-Alvarado C, Llaca-Díaz J, Flores-Aréchiga A, et al. Male urethritis. A review of the ideal diagnostic method. Uretritis masculina. Una revisión del método ideal de diagnóstico. Actas Urol Esp (Engl Ed). 2020;44(8):523-28. doi:10.1016/j.acuro.2019.11.008.
28. Bachmann LH, Manhart LE, Martin DH, et al. Advances in the Understanding and Treatment of Male Urethritis. Clin Infect Dis. 2015;61(Suppl 8):S763-69. doi:10.1093/cid/civ755.
29. Wu J, Ding C, Liu X, et al. Worldwide burden of genital human papillomavirus infection in female sex workers: a systematic review and meta-analysis. Int J Epidemiol. 2021;50(2):527-37. doi:10.1093/ije/dyaa289.
30. Sethi S, Ali A, Ju X, et al. A systematic review and meta-analysis of the prevalence of human papillomavirus infection in Indigenous populations — A Global Picture. J Oral Pathol Med. 2021;50(9):843-54. doi:10.1111/jop.13201.
31. Bray F, Ferlay J, Soerjomataram I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries [published correction appears in CA Cancer J Clin. 2020;70(4):313]. CA Cancer J Clin. 2018;68(6):394-424. doi:10.3322/caac.21492.
32. Das S, Doss CGP, Fletcher J, et al. The impact of human papilloma virus on human reproductive health and the effect on male infertility: An updated review. J Med Virol. 2023;95(4):e28697. doi:10.1002/jmv.28697.
33. Foresta C, Pizzol D, Moretti A, et al. Clinical and prognostic significance of human papillomavirus DNA in the sperm or exfoliated cells of infertile patients and subjects with risk factors. Fertil Steril. 2010;94(5):1723-27. doi:10.1016/j.fertnstert.2009.11.012.
34. Сыркашева А. Г., Долгушина Н.В., Яроцкая Е.Л. Влияние антропогенных химических веществ на репродукцию. Акушерство и гинекология. 2018;3:16- 21. doi:10.18565/aig.2018.3.16-21.
35. Сыркашева А. Г., Долгушина Н.В., Франкевич В.Е., Донников А.Е. Влияние тяжелых металлов на эффективность программ вспомогательных репродуктивных технологий в зависимости от полиморфизма генов системы детоксикации. Акушерство и гинекология. 2021;7:95-101. doi:10.18565/aig.2021.7.95-101.
36. Сыркашева А.Г., Киндышева С.В., Стародубцева Н.Л. и др. Бисфенол А в организме пациенток с бесплодием: влияние на результаты программ вспомогательных репродуктивных технологий. Акушерство и гинекология. 2021;5:113-20. doi:10.18565/aig.2021.5.113-120.
37. Rim KT. Reproductive Toxic Chemicals at Work and Efforts to Protect Workers’ Health: A Literature Review. Saf Health Work. 2017;8(2):143-50. doi:10.1016/j.shaw.2017.04.003.
38. Kumar S. Occupational and Environmental Exposure to Lead and Reproductive Health Impairment: An Overview. Indian J Occup Environ Med. 2018;22(3):128- 37. doi:10.4103/ijoem.IJOEM_126_18.
39. Doumouchtsis KK, Doumouchtsis SK, Doumouchtsis EK, Perrea DN. The effect of lead intoxication on endocrine functions. J Endocrinol Invest. 2009;32(2):175- 83. doi:10.1007/BF03345710.
40. Gandhi J, Hernandez RJ, Chen A, et al. Impaired hypothalamic-pituitarytesticular axis activity, spermatogenesis, and sperm function promote infertility in males with lead poisoning. Zygote. 2017;25(2):103-10. doi:10.1017/S0967199417000028.
41. Pizent A, Tariba B, Živković T. Reproductive toxicity of metals in men. Arh Hig Rada Toksikol. 2012;63(Suppl 1):35-46. doi:10.2478/10004-1254-63-2012-2151.
42. Massányi P, Massányi M, Madeddu R, et al. Effects of Cadmium, Lead, and Mercury on the Structure and Function of Reproductive Organs. Toxics. 2020;8(4):94. doi:10.3390/toxics8040094.
43. Bjørklund G, Chirumbolo S, Dadar M, et al. Mercury exposure and its effects on fertility and pregnancy outcome. Basic Clin Pharmacol Toxicol. 2019;125(4):317- 27. doi:10.1111/bcpt.13264.
44. Al-Saleh I, Shinwari N, Al-Amodi M. Accumulation of mercury in ovaries of mice after the application of skin-lightening creams. Biol Trace Elem Res. 2009;131(1):43-54. doi:10.1007/s12011-009-8341-x.
45. Schuurs AH. Reproductive toxicity of occupational mercury. A review of the literature. J Dent. 1999;27(4):249-56. doi:10.1016/s0300-5712(97)00039-0.
46. Henriques MC, Loureiro S, Fardilha M, Herdeiro MT. Exposure to mercury and human reproductive health: A systematic review. Reprod Toxicol. 2019;85:93-103. doi:10.1016/j.reprotox.2019.02.012.
47. Chen YW, Huang CF, Tsai KS, et al. Methylmercury induces pancreatic beta-cell apoptosis and dysfunction. Chem Res Toxicol. 2006;19(8):1080-85. doi:10.1021/tx0600705.
48. Davis BJ, Price HC, O’Connor RW, et al. Mercury vapor and female reproductive toxicity. Toxicol Sci. 2001;59(2):291-96. doi:10.1093/toxsci/59.2.291.
49. Choy CM, Lam CW, Cheung LT, et al. Infertility, blood mercury concentrations and dietary seafood consumption: a case-control study. BJOG. 2002;109(10):1121-25. doi:10.1111/j.1471-0528.2002.02084.x.
50. Choy CM, Yeung QS, Briton-Jones CM, et al. Relationship between semen parameters and mercury concentrations in blood and in seminal fluid from subfertile males in Hong Kong. Fertil Steril. 2002;78(2):426-28. doi:10.1016/s0015-0282(02)03232-6.
51. Zhou Y, Fu XM, He DL, et al. Evaluation of urinary metal concentrations and sperm DNA damage in infertile men from an infertility clinic. Environ Toxicol Pharmacol. 2016;45:68-73. doi:10.1016/j.etap.2016.05.020.
52. Lee S, Min JY, Min KB. Female Infertility Associated with Blood Lead and Cadmium Levels. Int J Environ Res Public Health. 2020;17(5):1794. doi:10.3390/ijerph17051794.
53. McClam M, Liu J, Fan Y, et al. Associations between exposure to cadmium, lead, mercury and mixtures and women’s infertility and long-term amenorrhea. Arch Public Health. 2023;81(1):161. doi:10.1186/s13690-023-01172-6.
54. Johnson MD, Kenney N, Stoica A, et al. Cadmium mimics the in vivo effects of estrogen in the uterus and mammary gland. Nat Med. 2003;9(8):1081-84. doi:10.1038/nm902.
55. Zhang Y, Li S, Li S. Relationship between cadmium content in semen and male infertility: a meta-analysis. Environ Sci Pollut Res Int. 2019;26(2):1947-53. doi:10.1007/s11356-018-3748-6.
56. Pfeiffenberger J, Beinhardt S, Gotthardt DN, et al. Pregnancy in Wilson’s disease: Management and outcome. Hepatology. 2018;67(4):1261-69. doi:10.1002/hep.29490.
57. Bhardwaj JK, Paliwal A, Saraf P. Effects of heavy metals on reproduction owing to infertility. J Biochem Mol Toxicol. 2021;35(8):e22823. doi:10.1002/jbt.22823.
58. Li Y, Gao Q, Li M, et al. Cadmium, Chromium, and Copper Concentration plus Semen-Quality in Environmental Pollution Site, China. Iran J Public Health. 2014;43(1):35-41.
59. Queiroz EK, Waissmann W. Occupational exposure and effects on the male reproductive system. Cad Saude Publica. 2006;22(3):485-93. doi:10.1590/s0102-311x2006000300003.
60. Sun HJ, Xiang P, Luo J, et al. Mechanisms of arsenic disruption on gonadal, adrenal and thyroid endocrine systems in humans: A review. Environ Int. 2016;95:61-68. doi:10.1016/j.envint.2016.07.020.
61. Jana K, Jana S, Samanta PK. Effects of chronic exposure to sodium arsenite on hypothalamo-pituitary-testicular activities in adult rats: possible an estrogenic mode of action. Reprod Biol Endocrinol. 2006;4:9. doi:10.1186/1477-7827-4-9.
62. Choudhury BP, Roychoudhury S, Sengupta P, et al. Arsenic-Induced Sex Hormone Disruption: An Insight into Male Infertility. Adv Exp Med Biol. 2022;1391:83-95. doi:10.1007/978-3-031-12966-7_6.
63. Kim YJ, Kim JM. Arsenic Toxicity in Male Reproduction and Development. Dev Reprod. 2015;19(4):167-80. doi:10.12717/DR.2015.19.4.167.
64. Xu W, Bao H, Liu F, et al. Environmental exposure to arsenic may reduce human semen quality: associations derived from a Chinese cross-sectional study. Environ Health. 2012;11:46. doi:10.1186/1476-069X-11-46.
65. Hsieh FI, Hwang TS, Hsieh YC, et al. Risk of erectile dysfunction induced by arsenic exposure through well water consumption in Taiwan. Environ Health Perspect. 2008;116(4):532-36. doi:10.1289/ehp.10930.
66. Sengupta M, Deb I, Sharma GD, Kar KK. Human sperm and other seminal constituents in male infertile patients from arsenic and cadmium rich areas of Southern Assam. Syst Biol Reprod Med. 2013;59(4):199-209. doi:10.3109/19396368.2013.783143.
67. Kong L, Tang M, Zhang T, et al. Nickel nanoparticles exposure and reproductive toxicity in healthy adult rats. Int J Mol Sci. 2014;15(11):21253-269. doi:10.3390/ijms151121253.
68. Forgacs Z, Massányi P, Lukac N, Somosy Z. Reproductive toxicology of nickel — review. J Environ Sci Health A Tox Hazard Subst Environ Eng. 2012;47(9):1249-60. doi:10.1080/10934529.2012.672114.
69. Pandey R, Srivastava SP. Spermatotoxic effects of nickel in mice. Bull Environ Contam Toxicol. 2000;64(2):161-167. doi:10.1007/s001289910025.
70. Yang J, Ma Z. Research progress on the effects of nickel on hormone secretion in the endocrine axis and on target organs. Ecotoxicol Environ Saf. 2021;213:112034. doi:10.1016/j.ecoenv.2021.112034.
71. Rizvi A, Parveen S, Khan S, Naseem I. Nickel toxicology with reference to male molecular reproductive physiology. Reprod Biol. 2020;20(1):3-8. doi:10.1016/j.repbio.2019.11.005.
72. Parveen S, Rizvi A, Naseem I. Nickel toxicity with reference to female reproductive physiology, pregnancy and teratogenesis: a brief review. Adv Chem Res. 2022;1:65-71. doi.org/10.37256/acbr.1220221464.
73. Wirth JJ, Rossano MG, Daly DC, et al. Ambient manganese exposure is negatively associated with human sperm motility and concentration. Epidemiology. 2007;18(2):270-73. doi:10.1097/01.ede.0000253939.06166.7e.
74. Li Y, Wu J, Zhou W, Gao E. Effects of manganese on routine semen quality parameters: results from a population-based study in China. BMC Public Health. 2012;12:919. doi:10.1186/1471-2458-12-919.
75. Yang H, Wang J, Yang X, et al. Occupational manganese exposure, reproductive hormones, and semen quality in male workers: A cross-sectional study. Toxicol Ind Health. 2019;35(1):53-62. doi:10.1177/0748233718810109.
76. Axmon A, Rylander L, Strömberg U, Hagmar L. Altered menstrual cycles in women with a high dietary intake of persistent organochlorine compounds. Chemosphere. 2004;56(8):813-19. doi:10.1016/j.chemosphere.2004.03.002.
77. Buck Louis GM, Dmochowski J, Lynch C, et al. Polychlorinated biphenyl serum concentrations, lifestyle and time-to-pregnancy. Hum Reprod. 2009;24(2):451-58. doi:10.1093/humrep/den373.
78. Toft G, Thulstrup AM, Jönsson BA, et al. Fetal loss and maternal serum levels of 2,2’,4,4’,5,5’-hexachlorbiphenyl (CB-153) and 1,1-dichloro-2,2-bis(p-chlorophenyl) ethylene (p,p’-DDE) exposure: a cohort study in Greenland and two European populations. Environ Health. 2010;9:22. doi:10.1186/1476-069X-9-22.
79. Grindler NM, Allsworth JE, Macones GA, et al. Persistent organic pollutants and early menopause in U.S. women. PLoS One. 2015;10(1):e0116057. doi:10.1371/journal.pone.0116057.
80. Meeker JD, Hauser R. Exposure to polychlorinated biphenyls (PCBs) and male reproduction. Syst Biol Reprod Med. 2010;56(2):122-131. doi:10.3109/19396360903443658.
81. Mumford SL, Kim S, Chen Z, et al. Persistent organic pollutants and semen quality: The LIFE Study. Chemosphere. 2015;135:427-35. doi:10.1016/j.chemosphere.2014.11.015.
82. Stukenborg JB, Mitchell RT, Söder O. Endocrine disruptors and the male reproductive system. Best Pract Res Clin Endocrinol Metab. 2021;35(5):101567. doi:10.1016/j.beem.2021.101567.
83. Paoli D, Giannandrea F, Gallo M, et al. Exposure to polychlorinated biphenyls and hexachlorobenzene, semen quality and testicular cancer risk. J Endocrinol Invest. 2015;38(7):745-52. doi:10.1007/s40618-015-0251-5.
84. Paul R, Moltó J, Ortuño N, et al. Relationship between serum dioxin-like polychlorinated biphenyls and post-testicular maturation in human sperm. Reprod Toxicol. 2017;73:312-21. doi:10.1016/j.reprotox.2017.07.004.
85. Bräuner EV, Lim YH, Koch T, et al. Endocrine Disrupting Chemicals and Risk of Testicular Cancer: A Systematic Review and Meta-analysis. J Clin Endocrinol Metab. 2021;106(12):e4834-e4860. doi:10.1210/clinem/dgab523.
86. Mori C, Nakamura N, Todaka E, et al. Correlation between human maternal-fetal placental transfer and molecular weight of PCB and dioxin congeners/isomers. Chemosphere. 2014;114:262-67. doi:10.1016/j.chemosphere.2014.04.095.
87. Mennigen JA, Thompson LM, Bell M, Tellez Santos M, Gore AC. Transgenerational effects of polychlorinated biphenyls: 1. Development and physiology across 3 generations of rats. Environ Health. 2018;17(1):18. doi:10.1186/s12940-018-0362-5.
88. Gore AC, Thompson LM, Bell M, Mennigen JA. Transgenerational effects of polychlorinated biphenyls: 2. Hypothalamic gene expression in rats†. Biol Reprod. 2021;105(3):690-704. doi:10.1093/biolre/ioab066.
89. Gillette R, Son MJ, Ton L, et al. Passing experiences on to future generations: endocrine disruptors and transgenerational inheritance of epimutations in brain and sperm. Epigenetics. 2018;13(10-11):1106-26. doi:10.1080/15592294.2018.1543506.
90. Kezios KL, Liu X, Cirillio PM, et al. Prenatal polychlorinated biphenyl exposure is associated with decreased gestational length but not birth weight: archived samples from the Child Health and Development Studies pregnancy cohort. Environ Health. 2012;11:49. doi:10.1186/1476-069X-11-49.
91. Lignell S, Aune M, Darnerud PO, et al. Prenatal exposure to polychlorinated biphenyls (PCBs) and polybrominated diphenyl ethers (PBDEs) may influence birth weight among infants in a Swedish cohort with background exposure: a cross-sectional study. Environ Health. 2013;12:44. doi:10.1186/1476-069X-12-44.
92. Papadopoulou E, Caspersen IH, Kvalem HE, et al. Maternal dietary intake of dioxins and polychlorinated biphenyls and birth size in the Norwegian Mother and Child Cohort Study (MoBa). Environ Int. 2013;60:209-16. doi:10.1016/j.envint.2013.08.017.
93. Caspersen IH, Haugen M, Schjølberg S, et al. Maternal dietary exposure to dioxins and polychlorinated biphenyls (PCBs) is associated with language delay in 3 year old Norwegian children. Environ Int. 2016;91:180-87. doi:10.1016/j.envint.2016.02.031.
94. Kristensen SL, Ramlau-Hansen CH, Ernst E, et al. Prenatal exposure to persistent organochlorine pollutants and female reproductive function in young adulthood. Environ Int. 2016;92-93:366-372. doi:10.1016/j.envint.2016.04.024.
95. Scheeres JJ, Chudley AE. Solvent abuse in pregnancy: a perinatal perspective. J Obstet Gynaecol Can. 2002;24(1):22-26. doi:10.1016/s1701-2163(16)30270-5.
96. Woodruff TJ, Carlson A, Schwartz JM, Giudice LC. Proceedings of the Summit on Environmental Challenges to Reproductive Health and Fertility: executive summary. Fertil Steril. 2008;89(2 Suppl):e1-e20. doi:10.1016/j.fertnstert.2008.01.065.
97. Hannigan JH, Bowen SE. Reproductive toxicology and teratology of abused toluene. Syst Biol Reprod Med. 2010;56(2):184-200. doi:10.3109/19396360903377195.
98. McDonald JC, Lavoie J, Côté R, McDonald AD. Chemical exposures at work in early pregnancy and congenital defect: a case-referent study. Br J Ind Med. 1987;44(8):527-33. doi:10.1136/oem.44.8.527.
99. Bianchi F, Cianciulli D, Pierini A, Seniori Costantini A. Congenital malformations and maternal occupation: a registry based case-control study. Occup Environ Med. 1997;54(4):223-28. doi:10.1136/oem.54.4.223.
100. García AM, Fletcher T. Maternal occupation in the leather industry and selected congenital malformations. Occup Environ Med. 1998;55(4):284-86. doi:10.1136/oem.55.4.284.
101. Chevrier C, Dananché B, Bahuau M, et al. Occupational exposure to organic solvent mixtures during pregnancy and the risk of non-syndromic oral clefts. Occup Environ Med. 2006;63(9):617-23. doi:10.1136/oem.2005.024067.
102. Cordier S, Ha MC, Ayme S, Goujard J. Maternal occupational exposure and congenital malformations. Scand J Work Environ Health. 1992;18(1):11-17. doi:10.5271/sjweh.1613.
103. McMartin KI, Chu M, Kopecky E, et al. Pregnancy outcome following maternal organic solvent exposure: a meta-analysis of epidemiologic studies. Am J Ind Med. 1998;34(3):288-92. doi:10.1002/(sici)1097-0274(199809)34:33.0.co;2-q.
104. Tikkanen J, Heinonen OP. Cardiovascular malformations and organic solvent exposure during pregnancy in Finland. Am J Ind Med. 1988;14(1):1-8. doi:10.1002/ajim.4700140102.
105. Kurppa K, Holmberg PC, Hernberg S, et al. Screening for occupational exposures and congenital malformations. Scand J Work Environ Health. 1983;9(2 Spec No):89-93. doi:10.5271/sjweh.2418.
106. Logman JF, de Vries LE, Hemels ME, et al. Paternal organic solvent exposure and adverse pregnancy outcomes: a meta-analysis. Am J Ind Med. 2005;47(1):37-44. doi:10.1002/ajim.20102.
107. Peretz J, Vrooman L, Ricke WA, et al. Bisphenol a and reproductive health: update of experimental and human evidence, 2007-2013. Environ Health Perspect. 2014;122(8):775-86. doi:10.1289/ehp.1307728.
108. Gore AC, Chappell VA, Fenton SE, et al. EDC-2: The Endocrine Society’s Second Scientific Statement on Endocrine-Disrupting Chemicals. Endocr Rev. 2015;36(6):E1-E150. doi:10.1210/er.2015-1010.
109. Braun JM, Kalkbrenner AE, Calafat AM, et al. Impact of early-life bisphenol A exposure on behavior and executive function in children. Pediatrics. 2011;128(5):873-82. doi:10.1542/peds.2011-1335.
110. Wang YX, You L, Zeng Q, et al. Phthalate exposure and human semen quality: Results from an infertility clinic in China. Environ Res. 2015;142:1-9. doi:10.1016/j.envres.2015.06.010.
111. Toft G, Jönsson BA, Lindh CH, et al. Association between pregnancy loss and urinary phthalate levels around the time of conception. Environ Health Perspect. 2012;120(3):458-63. doi:10.1289/ehp.1103552.
112. Huang PC, Kuo PL, Chou YY, et al. Association between prenatal exposure to phthalates and the health of newborns. Environ Int. 2009;35(1):14-20. doi:10.1016/j.envint.2008.05.012.
113. Swan SH, Sathyanarayana S, Barrett ES, et al. First trimester phthalate exposure and anogenital distance in newborns. Hum Reprod. 2015;30(4):963-72. doi:10.1093/humrep/deu363.
114. Braun JM, Kalkbrenner AE, Just AC, et al. Gestational exposure to endocrinedisrupting chemicals and reciprocal social, repetitive, and stereotypic behaviors in 4- and 5-year-old children: the HOME study. Environ Health Perspect. 2014;122(5):513-520. doi:10.1289/ehp.1307261.
115. Vélez MP, Arbuckle TE, Fraser WD. Maternal exposure to perfluorinated chemicals and reduced fecundity: the MIREC study. Hum Reprod. 2015;30(3):701- 9. doi:10.1093/humrep/deu350.
116. Gautam R, Priyadarshini E, Patel AK, Arora T. Assessing the impact and mechanisms of environmental pollutants (heavy metals and pesticides) on the male reproductive system: a comprehensive review. J Environ Sci Health C Toxicol Carcinog. 2024;42(2):126-53. doi:10.1080/26896583.2024.2302738.
117. Petrelli G, Figà-Talamanca I, Tropeano R, et al. Reproductive male-mediated risk: spontaneous abortion among wives of pesticide applicators. Eur J Epidemiol. 2000;16(4):391-93. doi:10.1023/a:1007630610911.
118. Hanke W, Jurewicz J. The risk of adverse reproductive and developmental disorders due to occupational pesticide exposure: an overview of current epidemiological evidence. Int J Occup Med Environ Health. 2004;17(2): 223-43.
119. Wu YQ, Rao M, Hu SF, et al. Effect of transient scrotal hyperthermia on human sperm: an iTRAQ-based proteomic analysis. Reprod Biol Endocrinol. 2020;18(1):83 doi:10.1186/s12958-020-00640-w.
120. Durairajanayagam D, Agarwal A, Ong C. Causes, effects and molecular mechanisms of testicular heat stress. Reprod Biomed Online. 2015;30(1):14-27. doi:10.1016/j.rbmo.2014.09.018.
121. Gong Y, Guo H, Zhang Z, et al. Heat Stress Reduces Sperm Motility via Activation of Glycogen Synthase Kinase-3α and Inhibition of Mitochondrial Protein Import. Front Physiol. 2017;8:718. doi:10.3389/fphys.2017.00718.
122. Shahat AM, Rizzoto G, Kastelic JP. Amelioration of heat stress-induced damage to testes and sperm quality. Theriogenology. 2020;158:84-96. doi:10.1016/j.theriogenology.2020.08.034.
123. Kim B, Park K, Rhee K. Heat stress response of male germ cells. Cell Mol Life Sci. 2013;70(15):2623-36. doi:10.1007/s00018-012-1165-4.
124. Bekkar B, Pacheco S, Basu R, DeNicola N. Association of Air Pollution and Heat Exposure With Preterm Birth, Low Birth Weight, and Stillbirth in the US: A Systematic Review [published correction appears in JAMA Netw Open. 2020 Jul 1;3(7):e2014510]. JAMA Netw Open. 2020;3(6):e208243. doi:10.1001/jamanetworkopen.2020.8243.
125. Chersich MF, Pham MD, Areal A, et al. Associations between high temperatures in pregnancy and risk of preterm birth, low birth weight, and stillbirths: systematic review and meta-analysis. BMJ. 2020;371:m3811. doi:10.1136/bmj.m3811.
126. Gaskins AJ, Mínguez-Alarcón L, VoPham T, et al. Impact of ambient temperature on ovarian reserve. Fertil Steril. 2021;116(4):1052-60. doi:10.1016/j.fertnstert.2021.05.091.
127. Tas S, Lauwerys R, Lison D. Occupational hazards for the male reproductive system. Crit Rev Toxicol. 1996;26(3):261-307. doi:10.3109/10408449609012525.
128. Figà-Talamanca I, Cini C, Varricchio GC, et al. Effects of prolonged autovehicle driving on male reproduction function: a study among taxi drivers. Am J Ind Med. 1996;30(6):750-58. doi:10.1002/(SICI)1097-0274(199612)30:63.0.CO;2-1
129. Zarei S, Dehghan SF, Vaziri MH, et al. Assessment of semen quality of taxi drivers exposed to whole body vibration. J Occup Med Toxicol. 2022;17(1):16. doi:10.1186/s12995-022-00357-z
130. Ogilvy-Stuart AL, Shalet SM. Effect of radiation on the human reproductive system. Environ Health Perspect. 1993;101 Suppl 2(Suppl 2):109-16. doi:10.1289/ehp.93101s2109.
131. Kumar S, Sharma A, Kshetrimayum C. Environmental & occupational exposure & female reproductive dysfunction. Indian J Med Res. 2019;150(6):532-545. doi:10.4103/ijmr.IJMR_1652_17.
132. Srivasatav S, Mishra J, Keshari P, et al. Impact of Radiation on Male Fertility. Adv Exp Med Biol. 2022;1391:71-82. doi:10.1007/978-3-031-12966-7_5.
133. Jangid P, Rai U, Sharma RS, Singh R. The role of non-ionizing electromagnetic radiation on female fertility: A review. Int J Environ Health Res. 2023;33(4):358- 73. doi:10.1080/09603123.2022.2030676.
134. Yildirim ME, Kaynar M, Badem H, et al. What is harmful for male fertility: cell phone or the wireless Internet? Kaohsiung J Med Sci. 2015;31(9):480-84. doi:10.1016/j.kjms.2015.06.006.
135. Agarwal A, Desai NR, Makker K, et al. Effects of radiofrequency electromagnetic waves (RF-EMW) from cellular phones on human ejaculated semen: an in vitro pilot study. Fertil Steril. 2009;92(4):1318-25. doi:10.1016/j.fertnstert.2008.08.022.
136. Negi P, Singh R. Association between reproductive health and nonionizing radiation exposure. Electromagn Biol Med. 2021;40(1):92-102. doi:10.1080/15368378.2021.1874973.
137. Budani MC, Tiboni GM. Ovotoxicity of cigarette smoke: A systematic review of the literature. Reprod Toxicol. 2017;72:164-81. doi:10.1016/j.reprotox.2017.06.184.
138. Talbot P, Riveles K. Smoking and reproduction: the oviduct as a target of cigarette smoke. Reprod Biol Endocrinol. 2005;3:52. doi:10.1186/1477-7827-3-52.
139. Dechanet C, Anahory T, Mathieu Daude JC, et al. Effects of cigarette smoking on reproduction. Hum Reprod Update. 2011;17(1):76-95. doi:10.1093/humupd/dmq033.
140. Augood C, Duckitt K, Templeton AA. Smoking and female infertility: a systematic review and meta-analysis. Hum Reprod. 1998;13(6):1532-39. doi:10.1093/humrep/13.6.1532.
141. Weinberg CR, Wilcox AJ, Baird DD. Reduced fecundability in women with prenatal exposure to cigarette smoking. Am J Epidemiol. 1989;129(5):1072-78. doi:10.1093/oxfordjournals.aje.a115211.
142. Waylen AL, Metwally M, Jones GL, et al. Effects of cigarette smoking upon clinical outcomes of assisted reproduction: a meta-analysis. Hum Reprod Update. 2009;15(1):31-44. doi:10.1093/humupd/dmn046.
143. Sadeu JC, Hughes CL, Agarwal S, Foster WG. Alcohol, drugs, caffeine, tobacco, and environmental contaminant exposure: reproductive health consequences and clinical implications. Crit Rev Toxicol. 2010;40(7):633-52. doi:10.3109/10408444.2010.493552.
144. Neal MS, Hughes EG, Holloway AC, Foster WG. Sidestream smoking is equally as damaging as mainstream smoking on IVF outcomes. Hum Reprod. 2005;20(9):2531-35. doi:10.1093/humrep/dei080.
145. Hughes EG, Brennan BG. Does cigarette smoking impair natural or assisted fecundity? Fertil Steril. 1996;66(5):679-89. doi:10.1016/s0015-0282(16)58618-x.
146. Sun L, Tan L, Yang F, et al. Meta-analysis suggests that smoking is associated with an increased risk of early natural menopause. Menopause. 2012;19(2):126-32. doi:10.1097/gme.0b013e318224f9ac.
147. Schoenaker DA, Jackson CA, Rowlands JV, Mishra GD. Socioeconomic position, lifestyle factors and age at natural menopause: a systematic review and metaanalyses of studies across six continents. Int J Epidemiol. 2014;43(5):1542-62. doi:10.1093/ije/dyu094.
148. Kapoor D, Jones TH. Smoking and hormones in health and endocrine disorders. Eur J Endocrinol. 2005;152(4):491-99. doi:10.1530/eje.1.01867.
149. Soldin OP, Makambi KH, Soldin SJ, O’Mara DM. Steroid hormone levels associated with passive and active smoking. Steroids. 2011;76(7):653-59. doi:10.1016/j.steroids.2011.02.042.
150. Zhao J, Leung JYY, Lin SL, Schooling MC. Cigarette smoking and testosterone in men and women: A systematic review and meta-analysis of observational studies. Prev Med. 2016;85:1-10. doi:10.1016/j.ypmed.2015.12.021.
151. Randolph JF Jr, Sowers M, Gold EB, et al. Reproductive hormones in the early menopausal transition: relationship to ethnicity, body size, and menopausal status. J Clin Endocrinol Metab. 2003;88(4):1516-22. doi:10.1210/jc.2002-020777.
152. Sowers MF, Beebe JL, McConnell D, et al. Testosterone concentrations in women aged 25-50 years: associations with lifestyle, body composition, and ovarian status. Am J Epidemiol. 2001;153(3):256-64. doi:10.1093/aje/153.3.256.
153. Gustafson O, Nylund L, Carlström K. Does hyperandrogenism explain lower in vitro fertilization (IVF) success rates in smokers? Acta Obstet Gynecol Scand. 1996;75(2):149-56. doi:10.3109/00016349609033308.
154. Ruan X, Mueck AO. Impact of smoking on estrogenic efficacy. Climacteric. 2015;18(1):38-46. doi:10.3109/13697137.2014.929106.
155. Hartz AJ, Kelber S, Borkowf H, et al. The association of smoking with clinical indicators of altered sex steroids--a study of 50,145 women. Public Health Rep. 1987;102(3):254-59.
156. Windham GC, Elkin EP, Swan SH, et al. Cigarette smoking and effects on menstrual function. Obstet Gynecol. 1999;93(1):59-65. doi:10.1016/s0029-7844(98)00317-2.
157. Hornsby PP, Wilcox AJ, Weinberg CR. Cigarette smoking and disturbance of menstrual function. Epidemiology. 1998;9(2):193-98.
158. Harlow SD, Park M. A longitudinal study of risk factors for the occurrence, duration and severity of menstrual cramps in a cohort of college women [published correction appears in Br J Obstet Gynaecol 1997 Mar;104(3):386]. Br J Obstet Gynaecol. 1996;103(11):1134-42. doi:10.1111/j.1471-0528.1996.tb09597.x.
159. Ju H, Jones M, Mishra GD. Smoking and trajectories of dysmenorrhoea among young Australian women. Tob Control. 2016;25(2):195-202. doi:10.1136/tobaccocontrol-2014-051920.
160. Hyland A, Piazza KM, Hovey KM, et al. Associations of lifetime active and passive smoking with spontaneous abortion, stillbirth and tubal ectopic pregnancy: a cross-sectional analysis of historical data from the Women’s Health Initiative. Tob Control. 2015;24(4):328-35. doi:10.1136/tobaccocontrol-2013-051458.
161. Bouyer J, Coste J, Shojaei T, et al. Risk factors for ectopic pregnancy: a comprehensive analysis based on a large case-control, population-based study in France. Am J Epidemiol. 2003;157(3):185-94. doi:10.1093/aje/kwf190.
162. Chow WH, Daling JR, Weiss NS, Voigt LF. Maternal cigarette smoking and tubal pregnancy. Obstet Gynecol. 1988;71(2):167-70.
163. Stergachis A, Scholes D, Daling JR, et al. Maternal cigarette smoking and the risk of tubal pregnancy. Am J Epidemiol. 1991;133(4):332-37. doi:10.1093/oxfordjournals.aje.a115885.
164. Soares SR, Simon C, Remohí J, Pellicer A. Cigarette smoking affects uterine receptiveness. Hum Reprod. 2007;22(2):543-47. doi:10.1093/humrep/del394.
165. Jukic AM, Weinberg CR, Baird DD, Wilcox AJ. The association of maternal factors with delayed implantation and the initial rise of urinary human chorionic gonadotrophin. Hum Reprod. 2011;26(4):920-26. doi:10.1093/humrep/der009.
166. Ersoy SG, Zhou Y, İnan H, et al. Cigarette Smoking Affects Uterine Receptivity Markers. Reprod Sci. 2017;24(7):989-95. doi:10.1177/1933719117697129.
167. Zdravkovic T, Genbacev O, Prakobphol A, et al. Nicotine downregulates the l-selectin system that mediates cytotrophoblast emigration from cell columns and attachment to the uterine wall. Reprod Toxicol. 2006;22(1):69-76. doi:10.1016/j.reprotox.2006.01.005.
168. Dai JB, Wang ZX, Qiao ZD. The hazardous effects of tobacco smoking on male fertility. Asian J Androl. 2015;17(6):954-60. doi:10.4103/1008-682X.150847.
169. Asare-Anane H, Bannison SB, Ofori EK, et al. Tobacco smoking is associated with decreased semen quality. Reprod Health. 2016;13(1):90. doi:10.1186/s12978-016-0207-z.
170. Zavos PM, Correa JR, Karagounis CS, et al. An electron microscope study of the axonemal ultrastructure in human spermatozoa from male smokers and nonsmokers. Fertil Steril. 1998;69(3):430-34. doi:10.1016/s0015-0282(97)00563-3.
171. Yeung CH, Tüttelmann F, Bergmann M, et al. Coiled sperm from infertile patients: characteristics, associated factors and biological implication. Hum Reprod. 2009;24(6):1288-1295. doi:10.1093/humrep/dep017.
172. Zalata AA, Ahmed AH, Allamaneni SS, et al. Relationship between acrosin activity of human spermatozoa and oxidative stress. Asian J Androl. 2004;6(4):313-18.
173. Shrivastava V, Marmor H, Chernyak S, et al. Cigarette smoke affects posttranslational modifications and inhibits capacitation-induced changes in human sperm proteins. Reprod Toxicol. 2014;43:125-29. doi:10.1016/j.reprotox.2013.12.001.
174. Gabrielsen JS, Tanrikut C. Chronic exposures and male fertility: the impacts of environment, diet, and drug use on spermatogenesis. Andrology. 2016;4(4):648- 61. doi:10.1111/andr.12198.
175. Taha EA, Ezz-Aldin AM, Sayed SK, et al. Smoking influence on sperm vitality, DNA fragmentation, reactive oxygen species and zinc in oligoasthenoteratozoospermic men with varicocele. Andrologia. 2014;46(6):687-91. doi:10.1111/and.12136.
176. Practice Committee of the American Society for Reproductive Medicine. Smoking and infertility: a committee opinion. Fertil Steril. 2012;98(6):1400-06. doi:10.1016/j.fertnstert.2012.07.1146.
177. Sharma R, Harlev A, Agarwal A, Esteves SC. Cigarette Smoking and Semen Quality: A New Meta-analysis Examining the Effect of the 2010 World Health Organization Laboratory Methods for the Examination of Human Semen. Eur Urol. 2016;70(4):635-45. doi:10.1016/j.eururo.2016.04.010.
178. Wilhoit LF, Scott DA, Simecka BA. Fetal Alcohol Spectrum Disorders: Characteristics, Complications, and Treatment. Community Ment Health J. 2017;53(6):711-18. doi:10.1007/s10597-017-0104-0.
179. Mutsaerts MA, Groen H, Huiting HG, et al. The influence of maternal and paternal factors on time to pregnancy--a Dutch population-based birth-cohort study: the GECKO Drenthe study. Hum Reprod. 2012;27(2):583-93. doi:10.1093/humrep/der429.
180. Hakim RB, Gray RH, Zacur H. Alcohol and caffeine consumption and decreased fertility [published correction appears in Fertil Steril 1999 May;71(5):974]. Fertil Steril. 1998;70(4):632-37. doi:10.1016/s0015-0282(98)00257-x.
181. Grodstein F, Goldman MB, Cramer DW. Infertility in women and moderate alcohol use. Am J Public Health. 1994;84(9):1429-32. doi:10.2105/ajph.84.9.1429.
182. Tolstrup JS, Kjaer SK, Holst C, et al. Alcohol use as predictor for infertility in a representative population of Danish women. Acta Obstet Gynecol Scand. 2003;82(8):744-49. doi:10.1034/j.1600-0412.2003.00164.x.
183. Gill J. The effects of moderate alcohol consumption on female hormone levels and reproductive function. Alcohol Alcohol. 2000;35(5):417-23. doi:10.1093/alcalc/35.5.417.
184. Becker U, Tønnesen H, Kaas-Claesson N, Gluud C. Menstrual disturbances and fertility in chronic alcoholic women. Drug Alcohol Depend. 1989;24(1):75-82. doi:10.1016/0376-8716(89)90012-4.
185. Kucheria K, Saxena R, Mohan D. Semen analysis in alcohol dependence syndrome. Andrologia. 1985;17(6):558-63. doi:10.1111/j.1439-0272.1985.tb01714.x.
186. Muthusami KR, Chinnaswamy P. Effect of chronic alcoholism on male fertility hormones and semen quality. Fertil Steril. 2005;84(4):919-24. doi:10.1016/j.fertnstert.2005.04.025.
187. Condorelli RA, Calogero AE, Vicari E, La Vignera S. Chronic consumption of alcohol and sperm parameters: our experience and the main evidences. Andrologia. 2015;47(4):368-79. doi:10.1111/and.12284.
188. Hassan MA, Killick SR. Negative lifestyle is associated with a significant reduction in fecundity. Fertil Steril. 2004;81(2):384-92. doi:10.1016/j.fertnstert.2003.06.027.
189. Mendiola J, Torres-Cantero AM, Vioque J, et al. A low intake of antioxidant nutrients is associated with poor semen quality in patients attending fertility clinics. Fertil Steril. 2010;93(4):1128-33. doi:10.1016/j.fertnstert.2008.10.075.
190. Wong WY, Zielhuis GA, Thomas CM, et al. New evidence of the influence of exogenous and endogenous factors on sperm count in man. Eur J Obstet Gynecol Reprod Biol. 2003;110(1):49-54. doi:10.1016/s0301-2115(03)00162-3.
191. Braga DP, Halpern G, Figueira Rde C, et al. Food intake and social habits in male patients and its relationship to intracytoplasmic sperm injection outcomes. Fertil Steril. 2012;97(1):53-59. doi:10.1016/j.fertnstert.2011.10.011.
192. Mendiola J, Torres-Cantero AM, Moreno-Grau JM, et al. Food intake and its relationship with semen quality: a case-control study. Fertil Steril. 2009;91(3):812- 18. doi:10.1016/j.fertnstert.2008.01.020.
193. Attaman JA, Toth TL, Furtado J, et al. Dietary fat and semen quality among men attending a fertility clinic. Hum Reprod. 2012;27(5):1466-74. doi:10.1093/humrep/des065.
194. Eslamian G, Amirjannati N, Rashidkhani B, et al. Intake of food groups and idiopathic asthenozoospermia: a case-control study. Hum Reprod. 2012;27(11):3328-36. doi:10.1093/humrep/des311.
195. Ricci E, Al-Beitawi S, Cipriani S, et al. Dietary habits and semen parameters: a systematic narrative review. Andrology. 2018;6(1):104-16. doi:10.1111/andr.12452.
196. Karayiannis D, Kontogianni MD, Mendorou C, et al. Association between adherence to the Mediterranean diet and semen quality parameters in male partners of couples attempting fertility. Hum Reprod. 2017;32(1):215-22. doi:10.1093/humrep/dew288.
197. Jurewicz J, Radwan M, Sobala W, et al. Dietary Patterns and Their Relationship With Semen Quality. Am J Mens Health. 2018;12(3):575-83. doi:10.1177/1557988315627139.
198. Afeiche MC, Williams PL, Gaskins AJ, et al. Meat intake and reproductive parameters among young men. Epidemiology. 2014;25(3):323-30. doi:10.1097/EDE.0000000000000092.
199. Calogero AE, Aversa A, La Vignera S, et al. The use of nutraceuticals in male sexual and reproductive disturbances: position statement from the Italian Society of Andrology and Sexual Medicine (SIAMS). J Endocrinol Invest. 2017;40(12):1389- 97. doi:10.1007/s40618-017-0699-6.
200. Showell MG, Brown J, Yazdani A, et al. Antioxidants for male subfertility. Cochrane Database Syst Rev. 2011;(1):CD007411. doi:10.1002/14651858.CD007411.pub2.
201. Chavarro JE, Rich-Edwards JW, Rosner BA, Willett WC. Protein intake and ovulatory infertility. Am J Obstet Gynecol. 2008;198(2):210.e1-210.e2107. doi:10.1016/j.ajog.2007.06.057.
202. Chavarro JE, Rich-Edwards JW, Rosner BA, Willett WC. Dietary fatty acid intakes and the risk of ovulatory infertility. Am J Clin Nutr. 2007;85(1):231-37. doi:10.1093/ajcn/85.1.231.
203. Chavarro JE, Rich-Edwards JW, Rosner BA, Willett WC. Use of multivitamins, intake of B vitamins, and risk of ovulatory infertility. Fertil Steril. 2008;89(3):668- 76. doi:10.1016/j.fertnstert.2007.03.089.
204. Chavarro JE, Rich-Edwards JW, Rosner BA, Willett WC. Diet and lifestyle in the prevention of ovulatory disorder infertility. Obstet Gynecol. 2007;110(5):1050-58. doi:10.1097/01.AOG.0000287293.25465.e1.
205. Practice Committee of the American Society for Reproductive Medicine. Definitions of infertility and recurrent pregnancy loss. Fertil Steril. 2008;90(5 Suppl):S60. doi:10.1016/j.fertnstert.2008.08.065.
206. Pasquali R, Pelusi C, Genghini S, et al. Obesity and reproductive disorders in women. Hum Reprod Update. 2003;9(4):359-72. doi:10.1093/humupd/dmg024.
207. Wise LA, Rothman KJ, Mikkelsen EM, et al. An internet-based prospective study of body size and time-to-pregnancy. Hum Reprod. 2010;25(1):253-64. doi:10.1093/humrep/dep360.
208. Gesink Law DC, Maclehose RF, Longnecker MP. Obesity and time to pregnancy. Hum Reprod. 2007;22(2):414-20. doi:10.1093/humrep/del400.
209. Jungheim ES, Travieso JL, Hopeman MM. Weighing the impact of obesity on female reproductive function and fertility. Nutr Rev. 2013;71 Suppl 1(0 1):S3-S8. doi:10.1111/nure.12056.
210. Metwally M, Tuckerman EM, Laird SM, et al. Impact of high body mass index on endometrial morphology and function in the peri-implantation period in women with recurrent miscarriage. Reprod Biomed Online. 2007;14(3):328-34. doi:10.1016/s1472-6483(10)60875-9.
211. Fedorcsák P, Dale PO, Storeng R, et al. Impact of overweight and underweight on assisted reproduction treatment. Hum Reprod. 2004;19(11):2523-28. doi:10.1093/humrep/deh485.
212. Clark AM, Ledger W, Galletly C, et al. Weight loss results in significant improvement in pregnancy and ovulation rates in anovulatory obese women. Hum Reprod. 1995;10(10):2705-12. doi:10.1093/oxfordjournals.humrep.a135772.
213. Kiddy DS, Hamilton-Fairley D, Bush A, et al. Improvement in endocrine and ovarian function during dietary treatment of obese women with polycystic ovary syndrome. Clin Endocrinol (Oxf). 1992;36(1):105-11. doi:10.1111/j.1365-2265.1992.tb02909.x.
214. Clark AM, Thornley B, Tomlinson L, et al. Weight loss in obese infertile women results in improvement in reproductive outcome for all forms of fertility treatment. Hum Reprod. 1998;13(6):1502-5. doi:10.1093/humrep/13.6.1502.
215. Sallmén M, Sandler DP, Hoppin JA, et al. Reduced fertility among overweight and obese men. Epidemiology. 2006;17(5):520-23. doi:10.1097/01.ede.0000229953.76862.e5.
216. Magnusdottir EV, Thorsteinsson T, Thorsteinsdottir S, et al. Persistent organochlorines, sedentary occupation, obesity and human male subfertility. Hum Reprod. 2005;20(1):208-15. doi:10.1093/humrep/deh569.
217. Jensen TK, Andersson AM, Jørgensen N, et al. Body mass index in relation to semen quality and reproductive hormones among 1,558 Danish men. Fertil Steril. 2004;82(4):863-70. doi:10.1016/j.fertnstert.2004.03.056.
218. Hammoud AO, Wilde N, Gibson M, et al. Male obesity and alteration in sperm parameters. Fertil Steril. 2008;90(6):2222-25. doi:10.1016/j.fertnstert.2007.10.011.
219. Martini AC, Tissera A, Estofán D, et al. Overweight and seminal quality: a study of 794 patients. Fertil Steril. 2010;94(5):1739-43. doi:10.1016/j.fertnstert.2009.11.017.
220. Chavarro JE, Toth TL, Wright DL, et al. Body mass index in relation to semen quality, sperm DNA integrity, and serum reproductive hormone levels among men attending an infertility clinic. Fertil Steril. 2010;93(7):2222-31. doi:10.1016/j.fertnstert.2009.01.100.
221. Kort HI, Massey JB, Elsner CW, et al. Impact of body mass index values on sperm quantity and quality. J Androl. 2006;27(3):450-52. doi:10.2164/jandrol.05124.
222. Corona G, Mannucci E, Schulman C, et al. Psychobiologic correlates of the metabolic syndrome and associated sexual dysfunction. Eur Urol. 2006;50(3):595- 604. doi:10.1016/j.eururo.2006.02.053.
223. Makhsida N, Shah J, Yan G, et al. Hypogonadism and metabolic syndrome: implications for testosterone therapy. J Urol. 2005;174(3):827-34. doi:10.1097/01.ju.0000169490.78443.59.
224. Winters SJ, Wang C, Abdelrahaman E, et al. Inhibin-B levels in healthy young adult men and prepubertal boys: is obesity the cause for the contemporary decline in sperm count because of fewer Sertoli cells? J Androl. 2006;27(4):560- 64. doi:10.2164/jandrol.05193.
225. Ghanayem BI, Bai R, Kissling GE, et al. Diet-induced obesity in male mice is associated with reduced fertility and potentiation of acrylamideinduced reproductive toxicity. Biol Reprod. 2010;82(1):96-104. doi:10.1095/biolreprod.109.078915.
226. Yen SS. Effects of lifestyle and body composition on the ovary. Endocrinol Metab Clin North Am. 1998;27(4):915-26. doi:10.1016/s0889-8529(05)70047-5.
227. Kirchengast S, Huber J. Body composition characteristics and fat distribution patterns in young infertile women. Fertil Steril. 2004;81(3):539-44. doi:10.1016/j.fertnstert.2003.08.018.
228. Hammiche F, Laven JS, Twigt JM, et al. Body mass index and central adiposity are associated with sperm quality in men of subfertile couples. Hum Reprod. 2012;27(8):2365-72. doi:10.1093/humrep/des177.
229. Vaamonde D, Da Silva-Grigoletto ME, García-Manso JM, et al. Physically active men show better semen parameters and hormone values than sedentary men. Eur J Appl Physiol. 2012;112(9):3267-73. doi:10.1007/s00421-011-2304-6.
230. Minas A, Fernandes ACC, Maciel Júnior VL, et al. Influence of physical activity on male fertility. Andrologia. 2022;54(7):e14433. doi:10.1111/and.14433.
231. Gebreegziabher Y, Marcos E, McKinon W, Rogers G. Sperm characteristics of endurance trained cyclists. Int J Sports Med. 2004;25(4):247-51. doi:10.1055/s-2004-819933.
232. Wise LA, Cramer DW, Hornstein MD, et al. Physical activity and semen quality among men attending an infertility clinic. Fertil Steril. 2011;95(3):1025-30. doi:10.1016/j.fertnstert.2010.11.006.
233. Jung A, Strauss P, Lindner HJ, Schuppe HC. Influence of moderate cycling on scrotal temperature. Int J Androl. 2008;31(4):403-407. doi:10.1111/j.1365-2605.2007.00783.x.
234. Hjollund NH, Storgaard L, Ernst E, et al. The relation between daily activities and scrotal temperature. Reprod Toxicol. 2002;16(3):209-14. doi:10.1016/s0890-6238(02)00026-6.
235. Redman LM. Physical activity and its effects on reproduction. Reprod Biomed Online. 2006;12(5):579-86. doi:10.1016/s1472-6483(10)61183-2.
236. Warren MP, Perlroth NE. The effects of intense exercise on the female reproductive system. J Endocrinol. 2001;170(1):3-11. doi:10.1677/joe.0.1700003.
237. Gudmundsdottir SL, Flanders WD, Augestad LB. Physical activity and fertility in women: the North-Trøndelag Health Study. Hum Reprod. 2009;24(12):3196-204. doi:10.1093/humrep/dep337.
238. Prior JC, Cameron K, Yuen BH, Thomas J. Menstrual cycle changes with marathon training: anovulation and short luteal phase. Can J Appl Sport Sci. 1982;7(3): 173-77.
239. Shangold MM, Levine HS. The effect of marathon training upon menstrual function. Am J Obstet Gynecol. 1982;143(8):862-69. doi:10.1016/0002-9378(82)90464-1.
240. Patterson DF. Menstrual dysfunction in athletes: assessment and treatment. Pediatr Nurs. 1995;21(3):227-310.
241. De Souza MJ, Metzger DA. Reproductive dysfunction in amenorrheic athletes and anorexic patients: a review. Med Sci Sports Exerc. 1991;23(9):995-1007.
242. Marshall LA. Clinical evaluation of amenorrhea in active and athletic women. Clin Sports Med. 1994;13(2):371-87.
243. Foucaut AM, Faure C, Julia C, et al. Sedentary behavior, physical inactivity and body composition in relation to idiopathic infertility among men and women. PLoS One. 2019;14(4):e0210770. doi:10.1371/journal.pone.0210770.
244. Fung TT, Hu FB, Yu J, et al. Leisure-time physical activity, television watching, and plasma biomarkers of obesity and cardiovascular disease risk. Am J Epidemiol. 2000;152(12):1171-78. doi:10.1093/aje/152.12.1171.
245. Sheiner EK, Sheiner E, Carel R, et al. Potential association between male infertility and occupational psychological stress. J Occup Environ Med. 2002;44(12):1093- 99. doi:10.1097/00043764-200212000-00001.
246. Clarke RN, Klock SC, Geoghegan A, Travassos DE. Relationship between psychological stress and semen quality among in-vitro fertilization patients. Hum Reprod. 1999;14(3):753-58. doi:10.1093/humrep/14.3.753.
247. Anderson K, Nisenblat V, Norman R. Lifestyle factors in people seeking infertility treatment — A review. Aust N Z J Obstet Gynaecol. 2010;50(1):8-20. doi:10.1111/j.1479-828X.2009.01119.x.
248. Eskiocak S, Gozen AS, Taskiran A, et al. Effect of psychological stress on the L-arginine-nitric oxide pathway and semen quality. Braz J Med Biol Res. 2006;39(5):581-88. doi:10.1590/s0100-879x2006000500003.
249. Lampiao F. Variation of semen parameters in healthy medical students due to exam stress. Malawi Med J. 2009;21(4):166-67. doi:10.4314/mmj.v21i4.49635.
250. Abu-Musa AA, Nassar AH, Hannoun AB, Usta IM. Effect of the Lebanese civil war on sperm parameters. Fertil Steril. 2007;88(6):1579-82. doi:10.1016/j.fertnstert.2007.01.067
251. Zorn B, Sucur V, Stare J, Meden-Vrtovec H. Decline in sex ratio at birth after 10- day war in Slovenia: brief communication. Hum Reprod. 2002;17(12):3173-77. doi:10.1093/humrep/17.12.3173
252. DeStefano F, Annest JL, Kresnow MJ, et al. Semen characteristics of Vietnam veterans. Reprod Toxicol. 1989;3(3):165-73. doi:10.1016/0890-6238(89)90003-8.
253. Jurewicz J, Hanke W, Sobala W, et al. Wpływ stresu zawodowego na jakość nasienia [The effect of stress on the semen quality]. Med Pr. 2010;61(6):607-13.
254. Fenster L, Katz DF, Wyrobek AJ, et al. Effects of psychological stress on human semen quality. J Androl. 1997;18(2):194-202.
255. Schneid-Kofman N, Sheiner E. Does stress effect male infertility — a debate. Med Sci Monit. 2005;11(8):SR11-SR13.
256. Althof SE, Needle RB. Psychological factors associated with male sexual dysfunction: screening and treatment for the urologist. Urol Clin North Am. 2011;38(2):141-46. doi:10.1016/j.ucl.2011.02.003.
257. Byun JS, Lyu SW, Seok HH, et al. Sexual dysfunctions induced by stress of timed intercourse and medical treatment. BJU Int. 2013;111(4 Pt B):E227-E234. doi:10.1111/j.1464-410X.2012.11577.x.
258. Sakamoto H, Matsuda K, Zuloaga DG, et al. Stress affects a gastrin-releasing peptide system in the spinal cord that mediates sexual function: implications for psychogenic erectile dysfunction. PLoS One. 2009;4(1):e4276. doi:10.1371/journal.pone.0004276.
259. Collins MM, Meigs JB, Barry MJ, et al. Prevalence and correlates of prostatitis in the health professionals follow-up study cohort. J Urol. 2002;167(3):1363-66.
260. Pontari MA, Ruggieri MR. Mechanisms in prostatitis/chronic pelvic pain syndrome. J Urol. 2004;172(3):839-45. doi:10.1097/01.ju.0000136002.76898.04.
261. Homan GF, Davies M, Norman R. The impact of lifestyle factors on reproductive performance in the general population and those undergoing infertility treatment: a review. Hum Reprod Update. 2007;13(3):209-23. doi:10.1093/humupd/dml056.
262. Louis GM, Lum KJ, Sundaram R, et al. Stress reduces conception probabilities across the fertile window: evidence in support of relaxation. Fertil Steril. 2011;95(7):2184-89. doi:10.1016/j.fertnstert.2010.06.078.
263. Hjollund NH, Jensen TK, Bonde JP, et al. Distress and reduced fertility: a followup study of first-pregnancy planners. Fertil Steril. 1999;72(1):47-53. doi:10.1016/s0015-0282(99)00186-7.
264. Smeenk JM, Verhaak CM, Vingerhoets AJ, et al. Stress and outcome success in IVF: the role of self-reports and endocrine variables. Hum Reprod. 2005;20(4):991-96. doi:10.1093/humrep/deh739.
265. Boivin J, Schmidt L. Infertility-related stress in men and women predicts treatment outcome 1 year later. Fertil Steril. 2005;83(6):1745-52. doi:10.1016/j.fertnstert.2004.12.039.
266. Pal L, Bevilacqua K, Santoro NF. Chronic psychosocial stressors are detrimental to ovarian reserve: a study of infertile women. J Psychosom Obstet Gynaecol. 2010;31(3):130-39. doi:10.3109/0167482X.2010.485258.
267. Campagne DM. Should fertilization treatment start with reducing stress? Hum Reprod. 2006;21(7):1651-58. doi:10.1093/humrep/del078.
268. Domar AD, Broome A, Zuttermeister PC, et al. The prevalence and predictability of depression in infertile women. Fertil Steril. 1992;58(6):1158-63.
269. Nelson CJ, Shindel AW, Naughton CK, et al. Prevalence and predictors of sexual problems, relationship stress, and depression in female partners of infertile couples. J Sex Med. 2008;5(8):1907-14. doi:10.1111/j.1743-6109.2008.00880.x.
270. Lakatos E, Szabó G, Szigeti FJ, Balog P. A pszichés jóllét, az életmód és a termékenység összefüggései [Relationships between psychological wellbeing, lifestyle factors and fertility]. Orv Hetil. 2015;156(12):483-92. doi:10.1556/OH.2015.30104.
271. Yusuf L. Depression, anxiety and stress among female patients of infertility; A case control study. Pak J Med Sci. 2016;32(6):1340-43. doi:10.12669/pjms.326.10828.
272. Rooney KL, Domar AD. The impact of stress on fertility treatment. Curr Opin Obstet Gynecol. 2016;28(3):198-201. doi:10.1097/GCO.0000000000000261.
273. Agarwal A, Aponte-Mellado A, Premkumar BJ, et al. The effects of oxidative stress on female reproduction: a review. Reprod Biol Endocrinol. 2012;10:49. doi:10.1186/1477-7827-10-49.
274. Prasad S, Tiwari M, Pandey AN, et al. Impact of stress on oocyte quality and reproductive outcome. J Biomed Sci. 2016;23:36. doi:10.1186/s12929-016-0253-4.
275. Nevšímalová S. Sleep and sleep-related disorders in women. Specifika spánku u žen a jeho poruch. Cas Lek Cesk. 2019;158(7-8):321-22.
276. Eisenberg E, Legro RS, Diamond MP, et al. Sleep Habits of Women With Infertility. J Clin Endocrinol Metab. 2021;106(11):e4414-e4426. doi:10.1210/clinem/dgab474.
277. Shechter A, Varin F, Boivin DB. Circadian variation of sleep during the follicular and luteal phases of the menstrual cycle. Sleep. 2010;33(5):647-56. doi:10.1093/sleep/33.5.647.
278. Kim SM, Neuendorff N, Alaniz RC, et al. Shift work cycle-induced alterations of circadian rhythms potentiate the effects of high-fat diet on inflammation and metabolism. FASEB J. 2018;32(6):3085-95. doi:10.1096/fj.201700784R.
279. Nam GE, Han K, Lee G. Association between sleep duration and menstrual cycle irregularity in Korean female adolescents. Sleep Med. 2017;35:62-6. doi:10.1016/j.sleep.2017.04.009.
280. Porwal A, Yadav YC, Pathak K, Yadav R. An Update on Assessment, Therapeutic Management, and Patents on Insomnia. Biomed Res Int. 2021;2021:6068952. doi:10.1155/2021/6068952.
281. Kang W, Jang KH, Lim HM, et al. The menstrual cycle associated with insomnia in newly employed nurses performing shift work: a 12-month follow-up study. Int Arch Occup Environ Health. 2019;92(2):227-35. doi:10.1007/s00420-018-1371-y.
282. Toffol E, Merikanto I, Lahti T, et al. Evidence for a relationship between chronotype and reproductive function in women. Chronobiol Int. 2013;30(6):756- 65. doi:10.3109/07420528.2012.763043.
283. Lawson CC, Johnson CY, Chavarro JE, et al. Work schedule and physically demanding work in relation to menstrual function: the Nurses’ Health Study 3. Scand J Work Environ Health. 2015;41(2):194-203. doi:10.5271/sjweh.3482.
284. Lawson CC, Whelan EA, Hibert LEN, et al. Rotating shift work and menstrual cycle characteristics. Epidemiology. 2011;22(3):305-12. doi:10.1097/EDE.0b013e3182130016.
285. Wang Y, Gu F, Deng M, et al. Rotating shift work and menstrual characteristics in a cohort of Chinese nurses. BMC Womens Health. 2016;16:24. doi:10.1186/s12905-016-0301-y.
286. Stocker LJ, Macklon NS, Cheong YC, Bewley SJ. Influence of shift work on early reproductive outcomes: a systematic review and meta-analysis. Obstet Gynecol. 2014;124(1):99-110. doi:10.1097/AOG.0000000000000321.
287. Hvidt JEM, Knudsen UB, Zachariae R, et al. Associations of bedtime, sleep duration, and sleep quality with semen quality in males seeking fertility treatment: a preliminary study. Basic Clin Androl. 2020;30:5. doi:10.1186/s12610-020-00103-7
288. Chen HG, Sun B, Chen YJ, et al. Sleep duration and quality in relation to semen quality in healthy men screened as potential sperm donors. Environ Int. 2020;135:105368. doi:10.1016/j.envint.2019.105368
289. Liu MM, Liu L, Chen L, et al. Sleep Deprivation and Late Bedtime Impair Sperm Health Through Increasing Antisperm Antibody Production: A Prospective Study of 981 Healthy Men. Med Sci Monit. 2017;23:1842-48. doi:10.12659/msm.900101.
290. Demirkol MK, Yıldırım A, Gıca Ş, et al. Evaluation of the effect of shift working and sleep quality on semen parameters in men attending infertility clinic. Andrologia. 2021;53(8):e14116. doi:10.1111/and.14116.
291. Liu K, Hou G, Wang X, et al. Adverse effects of circadian desynchrony on the male reproductive system: an epidemiological and experimental study. Hum Reprod. 2020;35(7):1515-28. doi:10.1093/humrep/deaa101.
292. Auger N, Healy-Profitós J, Wei SQ. In the arms of Morpheus: meta-analysis of sleep and fertility. Fertil Steril. 2021;115(3):596-98. doi:10.1016/j.fertnstert.2020.12.030.
293. Davis S, Lambrinoudaki I, Lumsden M, et al. Menopause. Nat Rev Dis Primers. 2015;1:15004. doi:10.1038/nrdp.2015.4.
294. Zervas IM, Lambrinoudaki I, Spyropoulou AC, et al. Additive effect of depressed mood and vasomotor symptoms on postmenopausal insomnia. Menopause. 2009;16(4):837-42. doi:10.1097/gme.0b013e318196063e.
295. Al-Safi ZA, Santoro N. Menopausal hormone therapy and menopausal symptoms. Fertil Steril. 2014;101(4):905-15. doi:10.1016/j.fertnstert.2014.02.032
296. Vivian-Taylor J, Hickey M. Menopause and depression: is there a link? Maturitas. 2014;79(2):142-46. doi:10.1016/j.maturitas.2014.05.014.
297. Bay-Jensen AC, Slagboom E, Chen-An P, et al. Role of hormones in cartilage and joint metabolism: understanding an unhealthy metabolic phenotype in osteoarthritis. Menopause. 2013;20(5):578-86. doi:10.1097/GME.0b013e3182745993.
298. Nappi RE, Kokot-Kierepa M. Vaginal Health: Insights, Views & Attitudes (VIVA) — results from an international survey. Climacteric. 2012;15(1):36-44. doi:10.3109/13697137.2011.647840.
299. Nappi RE, Palacios S. Impact of vulvovaginal atrophy on sexual health and quality of life at postmenopause. Climacteric. 2014;17(1):3-9. doi:10.3109/13697137.2013.871696.
300. Avis NE, Brockwell S, Randolph JF Jr, et al. Longitudinal changes in sexual functioning as women transition through menopause: results from the Study of Women’s Health Across the Nation. Menopause. 2009;16(3):442-52. doi:10.1097/gme.0b013e3181948dd0.
301. Shuster LT, Rhodes DJ, Gostout BS, et al. Premature menopause or early menopause: long-term health consequences. Maturitas. 2010;65(2):161-66. doi:10.1016/j.maturitas.2009.08.003.
302. Davis SR, Castelo-Branco C, Chedraui P, et al. Understanding weight gain at menopause. Climacteric. 2012;15(5):419-429. doi:10.3109/13697137.2012.707385.
303. Rocca WA, Grossardt BR, Miller VM, et al. Premature menopause or early menopause and risk of ischemic stroke. Menopause. 2012;19(3):272-77. doi:10.1097/gme.0b013e31822a9937.
304. Abramson BL, Melvin RG. Cardiovascular risk in women: focus on hypertension. Can J Cardiol. 2014;30(5):553-59. doi:10.1016/j.cjca.2014.02.014.
305. Lisabeth L, Bushnell C. Stroke risk in women: the role of menopause and hormone therapy [published correction appears in Lancet Neurol. 2012 Feb;11(2):125]. Lancet Neurol. 2012;11(1):82-91. doi:10.1016/S1474-4422(11)70269-1.
306. Weber MT, Maki PM, McDermott MP. Cognition and mood in perimenopause: a systematic review and meta-analysis. J Steroid Biochem Mol Biol. 2014;142:90- 98. doi:10.1016/j.jsbmb.2013.06.001.
307. Vermeulen A. Andropause. Maturitas. 2000;34(1):5-15. doi:10.1016/s0378-5122(99)00075-4.
308. McLachlan RI. The endocrine control of spermatogenesis. Baillieres Best Pract Res Clin Endocrinol Metab. 2000;14(3):345-62. doi:10.1053/beem.2000.0084.
309. Kidd SA, Eskenazi B, Wyrobek AJ. Effects of male age on semen quality and fertility: a review of the literature. Fertil Steril. 2001;75(2):237-48. doi:10.1016/s0015-0282(00)01679-4.
310. Fisch H, Goluboff ET, Olson JH, et al. Semen analyses in 1,283 men from the United States over a 25-year period: no decline in quality. Fertil Steril. 1996;65(5):1009-14. doi:10.1016/s0015-0282(16)58278-8.
311. Rolf C, Behre HM, Nieschlag E. Reproductive parameters of older compared to younger men of infertile couples. Int J Androl. 1996;19(3):135-42. doi:10.1111/j.1365-2605.1996.tb00451.x.
312. Vermeulen A, Goemaere S, Kaufman JM. "Sex Hormones, Body Composition and Aging." The Aging Male 2. 1999;1:8-15. doi:10.3109/13685539909003178.
313. Häkkinen K, Pakarinen A. Serum hormones and strength development during strength training in middle-aged and elderly males and females. Acta Physiol Scand. 1994;150(2):211-19. doi:10.1111/j.1748-1716.1994.tb09678.x.
314. Martin CE. Factor affecting sexual functioning in 60-79-year-old married males. Arch Sex Behav. 1981;10(5):399-420. doi:10.1007/BF01541434.
315. Tsitouras PD, Bulat T. The aging male reproductive system. Endocrinol Metab Clin North Am. 1995;24(2):297-15.
316. Bagatell CJ, Bremner WJ. Androgen and progestagen effects on plasma lipids. Prog Cardiovasc Dis. 1995;38(3):255-71. doi:10.1016/s0033-0620(95)80016-6.
317. Phillips GB, Pinkernell BH, Jing TY. The association of hypotestosteronemia with coronary artery disease in men. Arterioscler Thromb. 1994;14(5):701-706. doi:10.1161/01.atv.14.5.701.
318. Kapoor D, Malkin CJ, Channer KS, Jones TH. Androgens, insulin resistance and vascular disease in men. Clin Endocrinol (Oxf). 2005;63(3):239-50. doi:10.1111/j.1365-2265.2005.02299.x.
319. Zmunda JM, Thompson PD, Dickenson R, Bausserman LL. Testosterone decreases lipoprotein(a) in men. Am J Cardiol. 1996;77(14):1244-47. doi:10.1016/s0002-9149(96)00174-9.
320. Polderman KH, Stehouwer CD, van Kamp GJ, et al. Influence of sex hormones on plasma endothelin levels. Ann Intern Med. 1993;118(6):429-32. doi:10.7326/0003-4819-118-6-199303150-00006.
321. Caron P, Bennet A, Camare R, et al. Plasminogen activator inhibitor in plasma is related to testosterone in men. Metabolism. 1989;38(10):1010-1015. doi:10.1016/0026-0495(89)90014-0.
322. Ajayi AA, Mathur R, Halushka PV. Testosterone increases human platelet thromboxane A2 receptor density and aggregation responses. Circulation. 1995;91(11):2742-47. doi:10.1161/01.cir.91.11.2742.
323. Moffat SD. Effects of testosterone on cognitive and brain aging in elderly men. Ann N Y Acad Sci. 2005;1055:80-92. doi:10.1196/annals.1323.014.
324. Paulson JF, Bazemore SD. Prenatal and postpartum depression in fathers and its association with maternal depression: a meta-analysis. JAMA. 2010;303(19):1961- 1969. doi:10.1001/jama.2010.605.
325. Leach LS, Poyser C, Cooklin AR, Giallo R. Prevalence and course of anxiety disorders (and symptom levels) in men across the perinatal period: A systematic review. J Affect Disord. 2016;190:675686. doi:10.1016/j.jad.2015.09.063.
326. Skouteris H, Wertheim EH, Rallis S, et al. Depression and anxiety through pregnancy and the early postpartum: an examination of prospective relationships. J Affect Disord. 2009;113(3):303-308. doi:10.1016/j.jad.2008.06.002.
327. Philpott LF, Leahy-Warren P, FitzGerald S, Savage E. Stress in fathers in the perinatal period: A systematic review. Midwifery. 2017;55:113-27. doi:10.1016/j.midw.2017.09.016.
328. Goodman JH. Paternal postpartum depression, its relationship to maternal postpartum depression, and implications for family health. J Adv Nurs. 2004;45(1):26-35. doi:10.1046/j.1365-2648.2003.02857.x.
329. Genesoni L, Tallandini MA. Men’s psychological transition to fatherhood: an analysis of the literature, 1989-2008. Birth. 2009;36(4):305-18. doi:10.1111/j.1523-536X.2009.00358.x.
330. Hendrick V, Altshuler LL, Suri R. Hormonal changes in the postpartum and implications for postpartum depression. Psychosomatics. 1998;39(2):93-101. doi:10.1016/S0033-3182(98)71355-6.
331. Modak A, Ronghe V, Gomase KP, et al. A Comprehensive Review of Motherhood and Mental Health: Postpartum Mood Disorders in Focus. Cureus. 2023;15(9):e46209. doi:10.7759/cureus.46209.
332. Pearlstein T, Howard M, Salisbury A, Zlotnick C. Postpartum depression. Am J Obstet Gynecol. 2009;200(4):357-64. doi:10.1016/j.ajog.2008.11.033.
333. Mughal S, Azhar Y, Siddiqui W. Postpartum Depression. In: StatPearls. Treasure Island (FL): StatPearls Publishing; October 7, 2022.
334. Ali E. Women’s experiences with postpartum anxiety disorders: a narrative literature review. Int J Womens Health. 2018;10:237-49. doi:10.2147/IJWH.S158621.
335. Friedman SH, Reed E, Ross NE. Postpartum Psychosis. Curr Psychiatry Rep. 2023;25(2):65-72. doi:10.1007/s11920-022-01406-4.
336. Alstveit M, Severinsson E, Karlsen B. Readjusting one’s life in the tension inherent in work and motherhood. J Adv Nurs. 2011;67(10):2151-60. doi:10.1111/j.1365-2648.2011.05660.x.
337. Lynne J. Millward. The transition to motherhood in an organizational context: An interpretative phenomenological analysis. Journal of Occupational and Organizational Psychology. 2006; 79, 315-33. doi:10.1348/096317906X110322.
338. Alstveit M, Severinsson E, Karlsen B. Living on the edge of being overstretched--a Norwegian qualitative study of employed pregnant women. Health Care Women Int. 2010;31(6):533-51. doi:10.1080/07399331003611459
339. Campione W. Employed women’s well-being: the global and daily impact of work. Journal of Family and Economic Issues. 2008;29:346-61. doi:10.1007/s10834-008-9107-x.
340. Grice MM, Feda D, McGovern P, et al. Giving birth and returning to work: the impact of work-family conflict on women’s health after childbirth. Ann Epidemiol. 2007;17(10):791-98. doi:10.1016/j.annepidem.2007.05.002.
341. Hammer TH, Saksvik PØ, Nytrø K, et al. Expanding the psychosocial work environment: workplace norms and work-family conflict as correlates of stress and health. J Occup Health Psychol. 2004;9(1):83-97. doi:10.1037/1076-8998.9.1.83.
342. Öst CE, Wilhelmsson M. The long-term consequences of youth housing for childbearing and higher education. J Pol Model. 2019;41(5):845-58.
343. Sleebos J. OECD Social, Employment and Migration Working Papers, 2003. vol. 15. DELSA/ELSA/WD/SEM; 2003. Low fertility rates in OECD countries: facts and policy responses; pp. 1-63.
344. Cooke A, Mills TA, Lavender T. Advanced maternal age: delayed childbearing is rarely a conscious choice a qualitative study of women’s views and experiences. Int J Nurs Stud. 2012;49(1):30-9. doi:10.1016/j.ijnurstu.2011.07.013.
345. Peterson EWF. The role of population in economic growth. Sage Open. 2017;7(4).
346. Tavousi M, Motlagh ME, Eslami M, et al. Fertility desire among Iranians living in Tehran: reasons for desire and disinterest. J Iran Inst Health Sci Res. 2016;15(6):663-8.
347. Valashani TS, Alavijeh ZF, Heidari Z, Shoushtari ME. Ferility desire: facilitators and inhibitors. J Iran Inst Health Sci Res. 2019;18(3):241-9.
348. Wei J, Xue J, Wang D. Socioeconomic determinants of rural women’s desired fertility: A survey in rural Shaanxi, China. PLoS One. 2018;13(9):e0202968. doi:10.1371/journal.pone.0202968.
349. Whitley MD, Ro A, Choi B. Workplace breastfeeding support and job satisfaction among working mothers in the United States. Am J Ind Med. 2019;62(8):716-26. doi:10.1002/ajim.22989.
350. Sağlam YH, Özerdoğan N, Şahin MB, Gürsoy E. Workplace breastfeeding support for working women: A scale development study. Eur J Obstet Gynecol Reprod Biol X. 2023;20:100239. doi:10.1016/j.eurox.2023.100239.
351. Lin WT, Hsieh CC, Chang FC, et al. Effects of workplaces receiving "accreditation of health workplaces" on breastfeeding promotion, parental leave, and gender equality. J Occup Health. 2020;62(1):e12140. doi:10.1002/1348-9585.12140.
352. Ip S, Chung M, Raman G, et al. A summary of the Agency for Healthcare Research and Quality’s evidence report on breastfeeding in developed countries. Breastfeed Med. 2009;4 Suppl 1:S17-S30. doi:10.1089/bfm.2009.0050.
353. Sankar MJ, Sinha B, Chowdhury R, et al. Optimal breastfeeding practices and infant and child mortality: a systematic review and meta-analysis. Acta Paediatr. 2015;104(467):3-13. doi:10.1111/apa.13147.
354. Crouter AC, Head MR, McHale SM, Tucker CJ. Family time and the psychosocial adjustment of adolescent siblings and their parents. Journal of Marriage and Family. 2004;66(1):147-62. doi:10.1111/j.0022-2445.2004.00010.x-i1.
355. Duncan SC, Duncan TE, Strycker LA. Risk and protective factors influencing adolescent problem behavior: a multivariate latent growth curve analysis. Ann Behav Med. 2000;22(2):103-9. doi:10.1007/BF02895772.
356. Hofferth SL, Sandberg JF. How American children spend their time. Journal of Marriage and Family. 2001;63(2): 295-308. doi:10.1111/j.1741-3737.2001.00295.x.
357. Johnson MD, Galambos NL. Paths to intimate relationship quality from parent– adolescent relations and mental health. Journal of Marriage and Family. 2014;76(1):145-60. doi:10.1111/jomf.12074.
358. Dishion TJ, McMahon RJ. Parental monitoring and the prevention of child and adolescent problem behavior: a conceptual and empirical formulation. Clin Child Fam Psychol Rev. 1998;1(1):61-75. doi:10.1023/a:1021800432380.
359. Hawkins SS, Cole TJ, Law C; Millennium Cohort Study Child Health Group. Examining the relationship between maternal employment and health behaviours in 5-year-old British children. J Epidemiol Community Health. 2009;63(12):999-1004. doi:10.1136/jech.2008.084590.
360. Rosenbaum E, Morett CR. The effect of parents’ joint work schedules on infants’ behavior over the first two years of life: evidence from the ECLSB. Matern Child Health J. 2009;13(6):732-44. doi:10.1007/s10995-009-0488-8.
361. Clemans-Cope L, Perry CD, Kenney GM, et al. Access to and use of paid sick leave among low-income families with children. Pediatrics. 2008;122(2):e480-e486. doi:10.1542/peds.2007-3294.
362. Heymann SJ, Earle A. The impact of welfare reform on parents’ ability to care for their children’s health. Am J Public Health. 1999;89(4):502-5. doi:10.2105/ajph.89.4.502.
363. Torres AJC, Barbosa-Silva L, Oliveira-Silva LC, et al. The Impact of Motherhood on Women’s Career Progression: A Scoping Review of Evidence-Based Interventions. Behav Sci (Basel). 2024;14(4):275. doi:10.3390/bs14040275.
364. Hardoy I, Schøne P, Østbakken KM. Children and the gender gap in management. Labour Economics. 2017;47:124-37. doi:10.1016/j.labeco.2017.05.009.
365. Whittington A. Outdoor careers and motherhood. J Exp Educ. 2019;42:79-92. doi:10.1177/1053825918820354.
366. McIntosh B, McQuais R, Munro A, Dabir-Alai P. Motherhood and its impact on career progression. Gend. Manag. 2012;27:346-64. doi:10.1108/17542411211252651.
Об авторах
О. М. ДрапкинаРоссия
Драпкина Оксана Михайловна — академик РАН, д.м.н., профессор, директор ФГБУ "Национальный медицинский исследовательский центр терапии и профилактической медицины" Минздрава России, зав. кафедрой терапии и профилактической медицины ФГБОУ ВО "Российский университет медицины" Минздрава России
Москва
С. А. Орлов
Россия
К.м.н., с.н.с. отдела научно-стратегического развития первичной медико-санитарной помощи, руководитель лаборатории внедрения корпоративных программ ФГБУ "Национальный медицинский исследовательский центр терапии и профилактической медицины" Минздрава России
Москва
Р. Н. Шепель
Россия
К.м.н., зам. директора по перспективному развитию медицинской деятельности, руководитель отдела научно-стратегического развития первичной медико-санитарной помощи, ведущий научный сотрудник отдела научно-стратегического развития первичной медикосанитарной помощи, доцент кафедры общественного здоровья и организации здравоохранения ФГБУ "Национальный медицинский исследовательский центр терапии и профилактической медицины" Минздрава России, доцент кафедры терапии и профилактической медицины ФГБОУ ВО "Российский университет медицины" Минздрава России
Москва
А. В. Концевая
Россия
Д.м.н., доцент, зам. директора по научной и аналитической работе ФГБУ "Национальный медицинский исследовательский центр терапии и профилактической медицины" Минздрава России
Москва
О. И. Аполихин
Россия
Член-корреспондент РАН, д.м.н., профессор, директор НИИ урологии и интервенционной радиологии им. Н. А. Лопаткина — филиала ФГБУ "Национальный медицинский исследовательский центр радиологии" Минздрава России, главный внештатный специалист по репродуктивному здоровью мужчин Минздрава России
Москва
С. С. Красняк
Россия
К.м.н., в.н.с. отдела андрологии и репродукции человека НИИ урологии и интервенционной радиологии им. Н. А. Лопаткина — филиала ФГБУ "Национальный медицинский исследовательский центр радиологии" Минздрава России, ответственный секретарь Профильной комиссии Минздрава России по репродуктивному здоровью мужчин
Москва
Н. В. Долгушина
Россия
Д.м.н., профессор, заместитель директора по научной работе ФГБУ "Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени им. В. И. Кулакова" Минздрава России, главный внештатный специалист Минздрава России по репродуктивному здоровью женщин
Москва
И. В. Залата
Россия
Зав. отделом по развитию муниципальных и корпоративных программ БУЗ ВО "Вологодский областной центр общественного здоровья и медицинской профилактики"
Москва
Н. А. Лебедева
Россия
Главный внештатный специалист по медицинской профилактике Министерства здравоохранения Смоленской области, заведующий Центром общественного здоровья и медицинской профилактики ОГАУЗ "Смоленский областной врачебно-физкультурный диспансер" и медицинской профилактики (Смоленская область)
Москва
Г. П. Победенная
Россия
Д.м.н., профессор, главный внештатный специалист Министерства здравоохранения Луганской Народной Республики по терапии, зав. кафедрой внутренней медицины, пульмонологии и аллергологии Государственного учреждения Луганской Народной Республики "Луганский государственный медицинский университет имени Святителя Луки" (Луганская Народная Республика)
Москва
Ю. А. Шарапова
Россия
К.м.н., главный терапевт департамента здравоохранения Воронежской области, доцент кафедры госпитальной терапии и эндокринологии ФГБОУ ВО "Воронежский государственный медицинский университет им. Н. Н. Бурденко" Минздрава России
Москва
Рецензия
Для цитирования:
Драпкина ОМ, Орлов СА, Шепель РН, Концевая АВ, Аполихин ОИ, Красняк СС, Долгушина НВ, Залата ИВ, Лебедева НА, Победенная ГП, Шарапова ЮА. Сохранение и укрепление репродуктивного здоровья работающих граждан. Методические рекомендации. Первичная медико-санитарная помощь. 2024;1(1):81-133. https://doi.org/10.15829/3034-4123-2024-8. EDN: HTUNFA
For citation:
Drapkina OM, Orlov SA, Shepel RN, Kontsevaya AV, Apolikhin OI, Krasnyak SS, Dolgushina NV, Zalata IV, Lebedeva NA, Pobedennaya GP, Sharapova YA. Reproductive health promotion in working individuals. Guidelines. Primary Health Care (Russian Federation). 2024;1(1):81-133. (In Russ.) https://doi.org/10.15829/3034-4123-2024-8. EDN: HTUNFA
JATS XML























